Металлоксидной анод
Cтраница 1
Каталитические свойства металлоксидных анодов во многом определяются термодинамическими характеристиками оксидной фазы - энергиями связи кислорода на поверхности и в объеме, энергией образования дефектов, обусловленных нестехиометрией, энергиями активации движения ионов кислорода в решетке. Представления, развиваемые для каталитических процессов, во многом оправданы и для электрокатализа: чем выше энергия связи кислорода в оксиде, тем больше энергия активации окислительного процесса. [1]
Промышленное производство хлоратов организовано с применением графитовых, а также некоторых металлоксидных анодов. Наиболее существенным недостатком графитовых анодов является их значительный износ, который зависит от плотности тока, рН раствора и температуры. Показано, что износ графитовых анодов резко возрастает в интервале анодных плотностей тока 0 8 - 1 0 кА / м2, что соответствует превышению некоего критического потенциала, равного 1 6 В. Любое изменение условий электролиза, связанное с изменением потенциала графитового анода в сторону более положительных значений чем 1 6 В, вызывает резкое усиление износа. [2]
Промышленное производство хлоратов организовано с применением графитовых, а также некоторых металлоксидных анодов. Наиболее существенным недостатком графитовых анодов является их значительный износ, который зависит от плотности тока, рН раствора и температуры. Показано, что износ графитовых анодов резко возрастает в интервале анодных плотностей тока 0 8 - 1 0 кА / м2, что соответствует превышению некоего критического потенциала, равного 1 6 В. Любое изменение условий электролиза, связанное с изменением потенциала графитового анода в сторону более положительных значений чем 1 6 В, вызывает резкое усиление износа. [3]
 |
Сетчатый анод с алюминиевым токоподводом. [4] |
Таким образом удается, например, решить проблему токоподвода и равномерности распределения тока по поверхности такого слабоэлектропроводного металлоксидного анода, как магнетитовый. [5]
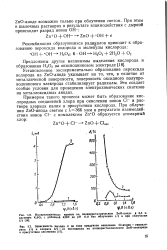
Установленное экспериментально образование пероксида водорода на ZnO-аноде указывает на то, что, в отличие от металлической поверхности, поверхность оксидного полупроводникового электрода стабилизирует радикалы. Это создает особые условия для проведения электрохимических синтезов на металлоксидных анодах. [7]
Страницы: 1