Анодные волны
Cтраница 1
Анодные волны хорошо выражены. Предельный ток пропорционален концентрации ионов свинца в растворе. [1]
Анодные волны наблюдаются в растворах, практически не содержащих ионов растворяемого металла. [2]
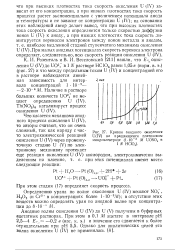 |
Кривая анодного окисления. [3] |
Анодные волны окисления U ( IV) до U ( V) получены в буферных ацетатных растворах. [4]
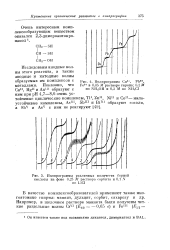 |
Полярограммы различных количеств борной кислоты на фоне 0 25 М раствора сорбита и 0 1 N по LiCl. [5] |
Исследованы анодные волны этого реагента, а также анодные и катодные волны образуемых им комплексов с металлами. [6]
Гидразин дает 2 анодных волны на Pt электроде, 2 5 H2SO4, при 0 5 и 1 0 В ( Нас. [7]
 |
Анодные, катодные кривые. [8] |
Приведенные здесь уравнения описывают анодные волны [ 5, 6 и 36 ] в растворах цианидов, сульфатов, тиосульфатов и роданидов. [9]
Почти во всех случаях анодные волны в растворах этих веществ, вызванные образованием нерастворимых солей со ртутью, осложняются адсорбцией и поэтому не подчиняются выведенным в этой главе уравнениям. Тем не менее анодные волны в растворах этих веществ широко используются в аналитических целях. [10]
Гидрохиноны или меркаптаны образуют анодные волны. [11]
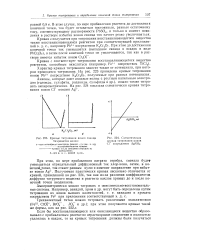 |
Кривые титрования ионов свинца бихроматом калия.| Схематическая кривая титрования ионов С1 - посредством AgNOs. [12] |
Анионы, которые дают анодные волны с ртутным капельным электродом ( галоиды, сульфиты, роданиды, сульфиды и др.), можно также титровать амперометрически. [13]
Почти во всех случаях анодные волны в растворах этих веществ, вызванные образованием нерастворимых солей со ртутью, осложняются адсорбцией и поэтому не подчиняются выведенным в этой главе уравнениям. Тем не менее анодные волны в растворах этих веществ широко используются в аналитических целях. [14]
Анализ проводили, регистрируя анодные волны хлоридов и иодидов и катодную волну бромида, которую получали после количественного окисления иона при контролируемом потенциале. Результаты определения хлоридов и бромидов совпадают с результатами, полученными классическими методами, иодид определяется с большой ошибкой, которая возрастает при уменьшении его концентрации. [15]
Страницы: 1 2 3 4