Функция - гран
Cтраница 1
Функция Грана линейна и обращается в ноль при значении У - F3KB только в том случае, когда S и Е сохраняют постоянные значения в процессе измерений. Изменение S и Е вносит в результат анализа существенную погрешность, причем с увеличением заряда определяемого иона погрешность возрастает: флуктуация S на уровне 2 % приводит к ошибке в 1 % для двухза-рядных ионов и 0 5 % - для однозарядных. [1]
По экспериментальным данным рассчитывали функцию Грана ( V0 V) - iQ - nE - K) t подставляя различные произвольно задаваемые значения / С. [3]
Левая часть выражения (7.38) является функцией Грана. [4]
Чувствительность и воспроизводимость потенциометрического титрования в определенной степени повышаются, если логарифмические ( потенциометриче-ские) кривые преобразуют с помощью функций Грана [2] в антилогарифмические и апроксимируют их прямыми линиями. Точку пересечения этих прямых с осью объемов и принимают за точку эквивалентности. Таким образом, этот метод сводится к оценке кривых линейного титрования экстраполяционным способом, которому присущи систематические ошибки [3], могущие достигать значительной величины. Правильные и воспроизводимые результаты могут быть получены подбором по методу наименьших квадратов таких параметров, как, например, точки эквивалентности, константы равновесия основной и побочных реакций для функции, интерполирующей данные титрования, с помощью ЭВМ. Однако алгоритмы этих методов очень сложны и вряд ли будут реализованы в ближайшее время в повседневной аналитической практике. [5]
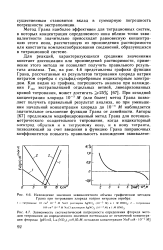
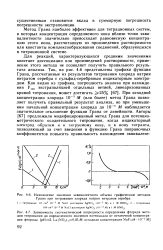
Для реакций, характеризующихся средними значениями констант диссоциации или произведений растворимости, применение этого метода не позволяет получить правильного результата анализа. Так, на рис. 4.6 представлены графики функции Грана, рассчитанные из результатов титрования хлорида натрия нитратом серебра с сульфид-серебряным индикаторным электродом. При исходной концентрации хлорида 10 - - 3 М ( или более) метод Грана позволяет получить правильный результат анализа, но при уменьшении начальной концентрации хлорида до 10 - 4 М наблюдается значительное отклонение функции Грана от линейности. [7]
Применение такой модели требует знания крутизны электродной функции и стандартного потенциала электрода, а также всех констант равновесия. Кроме того, применение линеаризованных функций требует большего объема расчетов, чем при использовании функций Грана. Однако в настоящее время компьютеры делают этот расчет не слишком обременительным. [8]
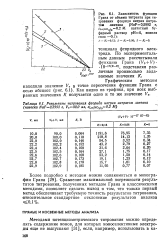
Уравнения (4.35) и (4.40) описывают кривую титрования после достижения точки эквивалентности. Для практического использования этого метода в уравнения (4.28), (4.35) и (4.40) вместо / С, - К6, являющихся алгебраической суммой констант, характеризующих систему, подставляют произвольное постоянное значение К, такое, чтобы получались значения функции Грана, удобные для графической интерпретации. В табл. 4.7 и на рис. 4.3 представлены результаты расчета функции Грана ( по экспериментальным результатам титрования фторида натрия солью лантана) и графического нахождения эквивалентного объема. [9]
 |
Графический вариант метода Грана при определении ионов методом многократных добавок. [10] |
Равенство (6.44) справедливо при условии, что при введении в раствор добавок ионная сила меняется незначительно, т.е. коэффициент активности определяемого иона можно считать постоянным. Применяя расчетный метод, исходят из того, что функция Грана линейна, следовательно, ее можно представить в виде уравнения прямой G ах Ь, т.е. ( Ух У) - Ют а. [11]
Уравнения (4.35) и (4.40) описывают кривую титрования после достижения точки эквивалентности. Для практического использования этого метода в уравнения (4.28), (4.35) и (4.40) вместо / С, - К6, являющихся алгебраической суммой констант, характеризующих систему, подставляют произвольное постоянное значение К, такое, чтобы получались значения функции Грана, удобные для графической интерпретации. В табл. 4.7 и на рис. 4.3 представлены результаты расчета функции Грана ( по экспериментальным результатам титрования фторида натрия солью лантана) и графического нахождения эквивалентного объема. [12]
Для реакций, характеризующихся средними значениями констант диссоциации или произведений растворимости, применение этого метода не позволяет получить правильного результата анализа. Так, на рис. 4.6 представлены графики функции Грана, рассчитанные из результатов титрования хлорида натрия нитратом серебра с сульфид-серебряным индикаторным электродом. При исходной концентрации хлорида 10 - - 3 М ( или более) метод Грана позволяет получить правильный результат анализа, но при уменьшении начальной концентрации хлорида до 10 - 4 М наблюдается значительное отклонение функции Грана от линейности. [14]
Современные аналитические приборы способны хранить в памяти значения откликов, полученных для градуировочных растворов, сравнивая их со значениями для анализируемого раствора и рассчитывая концентрацию определяемого вещества по заданному алгоритму с выдачей ее на дисплей прибора. Такие приборы позволяют своевременно выявлять и устранять грубые погрешности, корректировать наклон градуировочной зависимости и временной дрейф потенциала индикаторного электрода, а также учитывать поправку холостого опыта. В более сложных измерениях, требующих повышенной точности, используются компьютеры, контролирующие алгоритм собственно аналитического определения и обрабатывающие полученные данные, например по методу Грана. На экране дисплея можно отобразить также функцию погрешностей, по виду которой судят об отклонении функции Грана от прямолинейной зависимости и выбирают те ее части, которые наиболее близки к линейности. [15]
Страницы: 1 2