Диссоциация - чистая вода
Cтраница 1
Диссоциация чистой воды крайне мала и коэффициенты активности в уравнении ( II. [1]
При диссоциации чистой воды количество образующихся ионов водорода равно количеству ионов гидроксила, и такая среда называется нейтральной. В том случае, если в воде растворена какая-либо кислота, например серная, то за счет диссоциации кислоты концентрация ионов водорода в растворе будет много больше, чем в чистой воде, а концентрация гидроксильных ионов меньше. [2]
При диссоциации чистой воды количество образующихся ионов водорода равно количеству ионов гидроксида, такая среда называется нейтральной. В том случае, если в воде растворена какая-либо кислота, например серная, то за счет диссоциации кислоты активность ионов водорода в растворе будет много больше, чем в чистой воде, а активность гидроксид-ионов меньше. [3]
Теплота диссоциации чистой воды равна - & ffn при бесконечном разбавлении, но для конечных концентраций - ДЯ не имеет ясного физического смысла, так как при замене выражения срщв) срн ( М) - - рнв) - - рнм через ДЯв8) ( т-тт) молчаливо допускается, что срщмв) в нейтральном растворе соли равно сумме членов Фщм) и срН ( В), относящихся соответственно к растворам основания и кислоты. Мы лишены возможности проверить справедливость этого предположения, поскольку термодинамическим путем теплосодержания отдельных видов ионов не могут быть определены. [4]
 |
Схема движения ионов в электролитической ванне. [5] |
Степень диссоциации чистой воды очень мала. [6]
Если ионная сила р, в водном растворе электролита больше нуля, а коэффициент активности не равен единице, то упрощенное вычисление рН приводит к заметным отклонениям от действительных величин, так как в присутствии посторонних ионов истинная константа диссоциации чистой воды Ка не равна Кс. Вследствие того, что ан / н 1Н ], истинное значение водородного показателя равно раНрН - Hg / н Зная состав раствора, можно рассчитать его ионную силу и найти соответствующий коэффициент активности. Поскольку в качественном анализе не применяют точно отмеренных объемов реагентов и концентрации исследуемых растворов не превышают 0 01 - 0 05 М, можно производить расчеты без учета ионной силы раствора. [7]
При температуре 25 С лишь одна десятимиллионная часть t O диссоциирует на ионы; при этом образуется К) - 7 г-ионов водорода и 10 - 7 г-ионов гидроксила на каждую г-молекулу воды. С изменением температуры степень диссоциации чистой воды, а следовательно, и концентрации ионов Н и ОН - изменяются, оставаясь, естественно, равными друг другу. Произведение концентрации 2 свободных ионов Н и ОН -, находящихся в воде, является постоянной величиной для каждой температуры. Эта константа, обычно обозначаемая Kw, называется ионным произведением воды. [8]
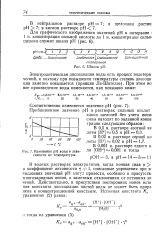 |
Изменение рН воды в зависимости от температуры. [9] |
В водных растворах электролитов, когда ионная сила ] а коэффициент активности f ф 1, описанные упрощения при в1 числениях значений рН могут привести, особенно в присутств. Действительно, в присутствии посторонних ионов исти ная константа диссоциации чистой воды не может быть прира пена к концентрационной константе. [10]
По теории диссоциации, процесс нейтрализации при смешении сильной кислоты и сильного основания состоит в том, что Н - ионы кислоты и ОН - - ионы основания образуют недиссоциированную воду. Как только ОН - и Н приходят в соприкосновение, то, по закону действия масс, должно наступить равновесие между произведением их концентраций и концентрацией недиссоциированной воды, которое определяется величиной константы диссоциации чистой воды. Так как в разбавленном водном растворе концентрацию недиссоциированной воды можно принять ( приблизительно) за постоянную, то практически все добавленные к воде Н и ОН - должны исчезнуть, ибо значение уже существующего в чистой воде произведения ионов не может быть изменено. До смешения растворов основания и кислоты мы имеем положительные ионы основания, ОН -, ионы кислотного остатка и Н, а после смешения только положительные ионы основания и отрицательные ионы кислотного остатка, которые образуют ( сильно диссоциированную) соль; эти ионы не принимали никакого участия в процессе нейтрализации. Кислотный и основной радикалы не играют, следовательно, никакой роли, и поэтому теплота нейтрализации всех сильно диссоциированных однокислотных оснований и одноосновных кислот одинакова; значение ее, при температуре t равное 14617 - 48 5 t кал. ОН - в недиссоциированную воду при 0 освобождается 14617 кал. Эту теп юту диссоциации не с едует смешивать с той, которая набчюдается при соединении газообразных водорода и кислорода в водяной пар. [11]
По закону действия масс произведение Н на ОН -, деленное на конаентрашш недиссоциированной воды, должно быть постоянным. Отсюда еле ует, что произведение ионов также должно иметь всегда постоянное значе; ие. Отсюда мы непосредственно находим степень диссоциации чистой воды Произведениз ионов должно иметь в чистой воде то же значение, концентрации же Н и ОН - равны. [12]
Страницы: 1