Электролитическая диссоциация - соединение
Cтраница 1
 |
Схема ориентации молекул воды в электростатическом поле, созда-ваемом ионами хлорида натрия. [1] |
Электролитическая диссоциация соединений зависит как от характера химических связей в них, так и от характера растворителя. [2]
Мы видим, таким образом, что наличие электролитической диссоциации соединений, с которыми мы имеем дело при анализе, весьма облегчает последний. В действительности же облегчение это оказывается значительно большим, чем было отмечено выше. В самом деле, количество наиболее важных катионов невелико, примерно около 25; приблизительно столько же и наиболее известных анионов. [3]
Ожигающее действие препаратов обусловлено ионами водорода в рабочем растворе и зависит от степени электролитической диссоциации соединений. В связи с этим недопустимо наличие в препаратах избыточного количества свободных минеральных кислот и кислых солей. Для растений опасны также непредельные углеводороды и ароматические соединения, содержащиеся в минеральных маслах. [4]
Определения кислот и оснований, учитывающие электролитическую диссоциацию соединений в растворе, были даны С. [5]
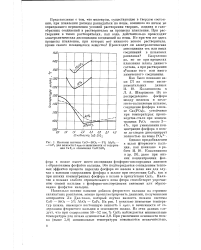 |
Изокомы системы CaO - SiC2 - 5 % AUOg - - CaFa для вязкости 5 пуаз в зависимости от содержания CaF2 и отношения CaO. Si02. [6] |
Представление о том, что молекулы, существующие в твердом состоянии, при плавлении должны распадаться на ионы, возникло из ничем не оправданного перенесения условий растворения твердых, жидких и газообразных соединений в растворителях на процессы плавления. При растворении в таких растворителях, как вода, действительно происходит электролитическая диссоциация соединений на ионы. [7]
Раствор далее нагреем до полного растворения кристаллов, а затем охладим и отделим выпавший осадок. Полученные кристаллы SrC2O4 - H2O содержат - 89Sr, что объясняется электролитической диссоциацией соединений стронция в водном растворе. [8]
Одним из самых универсальных растворителей является вода. Она растворяет многие твердые, жидкие, газообразные, органические и неорганические вещества. В отличие от других растворов водные растворы солей, кислот и оснований обладают способностью хорошо проводить электрический ток. Вещества, проводящие в растворе электрический ток, называют электролитами, причем электрическая проводимость электролитов определяется не свободными электронами, как в металлах, а гидратированными ионами - катионами и анионами, которые образуются в результате электролитической диссоциации соединений в воде. Учение, объясняющее и количественно описывающее такие процессы, получило название теории электролитической диссоциации. Важнейшая особенность воды как растворителя заключается в том, что ее молекулы полярны и имеют большой электрический момент диполя и-произведение величины зарядов на расстояние между ними. [9]
С 1945 работал в Ин-те общей и неорганической химии АН УССР. Основные научные исследования посвящены химии минералов и электрохимии неводных растворов. Обосновал связь между степенью электролитической диссоциации соединений и их способностью к комплексо-образованию в растворах и тем самым экспериментально подтвердил химическую теорию растворов Менделеева. [10]
Страницы: 1