Ингибирование - наводороживание
Cтраница 1
Ингибирование наводороживания алифатическими спиртами имеет место только в ограниченной области катодной поляризации. [1]
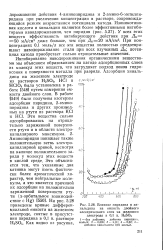 |
Влияние пиридина и хи. [2] |
Ингибирование наводороживания органическими веществами мы объясняем образованием на катоде адсорбционных слоев из молекул этих веществ, что затрудняет подход ионов гидро-ксония к поверхности металла при разряде. Адсорбция хиналь-дина на железном электроде из растворов H2SO4, НС1 и с мкФ / см - НС1О4 была установлена в работе [ 5481 путем измерения емкости двойного слоя. Эти вещества сильно адсорбировались на отрицательно заряженной поверхности ртути и в области электрокапиллярного максимума. Аминопиридин понижает также положительную ветвь электрокапиллярной кривой, несмотря на наличие положительного заряда у молекул этих веществ в кислой среде. [3]
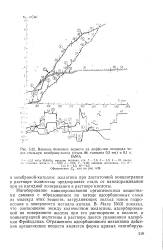 |
Влияние белковых веществ на диффузию водорода через стальную мембрану-катод ( сталь 08, толщина 0 3 мм в 0 1 н. [4] |
Ингибирование наводороживания органическими веществами связано с образованием на катоде адсорбционных слоев из молекул этих веществ, затрудняющих подход ионов гидро-ксония к поверхности металла катода. Маху [563] показал, что соотношение между количеством желатины, адсорбированной на поверхности железа при его растворении в кислоте, и концентрацией желатины в растворе дается уравнением адсорбции Фрейндлиха. [5]
Это обстоятельство указывает на то, что ингибирование наводороживания зависит от силы связи хемосорбции амина с металлом катода, поскольку сила связи хемосорбции определяется электронной структурой металла и энергией ионизации ингибитора, или его способностью отдавать свои электроны металлу; чем больше эта способность, тем сильнее хемосорбция. [6]
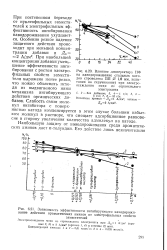 |
Зависимость эффективности ингибирующего наводорожи-вание действия ароматических аминов от электрофильяых свойств. [7] |
При постепенном переходе от нуклеофильных замести - S телей к электрофильным эффективность ингибирования наводороживания ухудшается. [8]
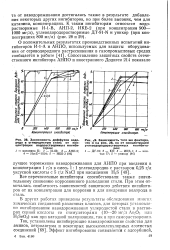 |
Зависимость диффузии водорода в углеродистую сталь от концентрации водорастворимых ингибиторов.| Зависимость того же фактора, что и на 28, но от концентрации углеводородорастворимых ингибиторов. [9] |
В других работах приведены результаты обследования многих химических соединений различных классов, для которых установлено ингибирование наводороживания углеродистой стали в растворах серной кислоты со стимуляторами ( 10 - 20 мг / л As2O3 или Н25еОз) как при катодной поляризации, так и при саморастворении. [10]
При больших Дк, ведущих к смещению заряда поверхности железного электрода в отрицательную сторону, наступает десорбция анионов арабовой кислоты и ингибирование наводороживания железа становится невозможным. [11]
Чем меньше время жизни адмолекулы ингибитора, тем больше вероятность попадания на освобождающиеся адсорбционные центры адатомов Н, таким образом, имеются теоретические ограничения эффективности органических ингибиторов наводороживания. Поэтому, по-видимому, практически и не удается достичь 100 % ингибирования наводороживания. [12]
ПАВ в виде смеси близких по составу гомологов используют в качестве смачивающих ( антипиттин-говых), сглаживающих и блескообразующих добавок. В этом случае возможно использование некоторых добавок ПАВ к электролитам для улучшения служебных характеристик металла покрытия и достижения эффекта ингибирования наводороживания стальной основы. Добавка 10 г / л полиэтиленгликоля М2000 в сульфатный электролит кадмирования [ CdSO4 - 8 / 3H2O ( 100 г / л); Н3ВО3 ( 20 г / л); NaCl ( 30 г / л); рН 4 5 ] увеличивает пластичность при скручивании проволоки из стали У8А на 14 % ( при 6Са 20 мкм и DK - 1 А / дма), а в сульфатно-аммониевом электролите CdO ( 30 г / л); ( NH4) 2SO4 ( 300); Н2ВО3 ( 20); рН 6 81 приводит к почти полному предотвращению наводороживания. [13]
Величина адсорбции органического вещества на катоде зависит от знака заряда поверхности катода, структуры и состояния молекул органического вещества в при-электродном слое раствора электролита. В случае карбоновых кислот мы имеем молекулы, способные адсорбироваться лишь в небольшом интервале потенциалов вблизи точки нулевого заряда металла катода; в случае аминов на катоде адсорбируются положительно заряженные ионы и эта адсорбция простирается на область отрицательных зарядов поверхности катода. У аминокислот эффективность ингибирования наводороживания сильно падает с увеличением Дк, вызывающим увеличение отрицательного заряда поверхности катода. Аминокислоты благодаря наличию основных и кислотных групп являются амфоли-тами. Аланин, имеющий близкие константы ионизации, дает такое же соотношение катионной и цвиттерионной форм. Вероятно, ухудшение защитного действия аминокислот при увеличении отрицательного заряда поверхности катода объясняется взаимодействием с поверхностью катода отрицательно заряженных карбоксильных групп цвиттерионов. Адсорбция аминокислот на железном катоде происходит за счет взаимодействия аминогрупп с поверхностью катода. [14]
Страницы: 1