Ингибирование - электродный процесс
Cтраница 1
Ингибирование электродных процессов органическими веществами было количественно исследовано на стационарном и капельном ртутных электродах. [1]
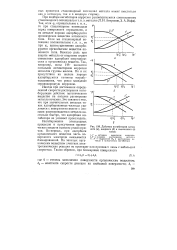 |
Действие ингибиторов катодного ( а, анодного ( б и смешанного ( в типов. [2] |
Ингибирование электродных процессов в присутствии органических веществ вызвано рядом причин. Во-первых, при адсорбции органического вещества часть поверхности электрода оказывается блокированной. На занятых органическим веществом участках электрохимическая реакция не протекает или протекает лишь с небольшой скоростью. [3]
 |
Зависимость токов восстановления катиона феррициния вводном 0 М растворе НС1О4 от концентрации борофторнда феррициния при потенциалах-0 2 ( / и - 1 1 в ( 2 ( по данным 1. [4] |
В области потенциалов максимального ингибирования электродного процесса показатель степени х0 85, что также близко соответствует процессам, кинетика которых определяется скоростью обновления поверхности ртутного электрода. Даже токи при потенциалах отрицательнее - 1 0 в при достаточно высокой концентрации соли феррициния не удовлетворяют в полной мере критериям чисто диффузионных токов. [5]
Адсорбция органического растворителя на электроде может вызвать ингибирование электродного процесса и изменение потенциала. Природа растворителя оказывает также существенное влияние на равновесие в растворе. Во-первых, сам растворитель в той или иной степени является комплексообразователем, и во-вторых, происходит изменение взаимодействий между анионами и катионами, присутствующими в растворе. [6]
Адсорбция нейтральных органических веществ обычно ведет к ингибированию электродного процесса. По Фрумкину [43], можно ожидать, что механизм ингиби-рования может меняться при переходе от 0, близкой к нулю, до практически полного покрытия электрода. [7]
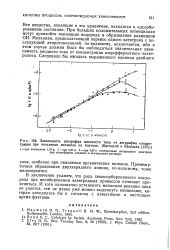 |
Зависимость логарифма плотности тока от логарифма концентрации при окислении метанола на платине. ( Багоцкий и Васильев. [8] |
В заключение укажем, что роль хемосорбированного кислорода при ингибировании электродных процессов начинает проясняться. И хотя однозначно установить механизм реакции пока не удается, тем не менее уже можно выдвинуть концепцию, которая находилась бы в согласии с известными в настоящее время фактами. [9]
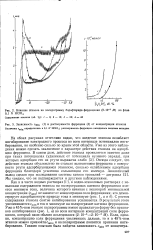 |
Зависимость cmin ( 1 и растворимости ферроцена ( 2 от концентрации этанола Величины cmin определялись в 0 1 N НСЮ4. растворимость ферроцена находилась весовым методой. [10] |
На обоих рисунках отчетливо видно, что введение этанола ослабляет ингибирование электродного процесса во всем интервале потенциалов инги-бирования, но особенно сильно по краям этой области. [11]
При исследовании адсорбционных явлений в системе катион тропилий - дитропил [11-13] особенно четко наблюдалось ослабление ингибирования электродного процесса адсорбирован - ным продуктом добавками к раствору посторонних поверхностно-активных веществ. Опыт показывает, что добавки поверхностно-активных веществ оказывают сильное влияние и на поляро-грамму катиона феррициния. [12]
Вещества первых двух групп инги-бируют электродные процессы, вещества третьей группы их промоти-руют. Ингибирование электродных процессов обусловлено адсорбцией ПАВ. Их применение представляет интерес для нанесения высокотемпературных гальванических покрытий. [13]
Эти же рассуждения справедливы для случая образования пленки. Появление второй постояннотоковой волны указывает на ингибирование электродного процесса, когда поверхность электрода полностью покрывается пленкой продукта реакции. Так как при коротких периодах капания скорость образования поверхности выше, то концентрация продукта реакции, при которой поверхность электрода покроется полностью, должна быть выше в скоростных условиях. Например, для сульфида в классических условиях ( 2 9с) вторая волна появляется при концентрации 3 - Ю 4 М, а при периоде капания 0 16 с ее не видно до концентрации 7 - Ю-4 А. [14]
Вероятно, в полярографии нет более неприятных явлений, чем адсорбция или образование пленки; они часто ассоциируются со словами плохие новости. В постояннотоковой полярографии адсорбции и образованию пленок часто приписывают максимумы, нарушение капания, нелинейность калибровочных кривых, ингибирование электродного процесса, расщепление или растяжение волн и другие аналитически нежелательные эффекты. В статьях [31 - 38] приведены некоторые примеры влияния поверхностных явлений. В последующих главах будут представлены и обсуждены конкретные примеры. [15]
Страницы: 1