Химический индивид
Cтраница 2
При определении объема понятия химический индивид целесообразно исходить из более общего представления о фазе и рассматривать как сложные, так и простые вещества. [16]
Вторая категория объединила те химические индивиды, которые не могут быть характеризованы присутствием дальтонов-ских точек и, следовательно, не подчиняются закону постоянных и кратных пропорций, хотя и могут обладать плоскими максимумами на кривой плавкости. Эти соединения Н. С. Курна-ковым были названы бертоллидами. [17]
Термином сложные химические соединения определяют химические индивиды, содержащие три и более компонентов. Если простых веществ ( с учетом аллотропии и полиморфизма) насчитывается около 200, а бинарных соединений - порядка 10 000, сложных многокомпонентных соединений значительно больше. Традиционно эти объекты подразделяют на 3 класса: основания, кислоты и соли. [18]
Термином сложные химические соединения определяют химические индивиды, содержащие три элемента и более. Если простых веществ ( с учетом аллотропии и полиморфизма) насчитывается около 200, а бинарных соединений - порядка 10 000, то сложных химических соединений значительно больше. Традиционно эти объекты подразделяются на три класса: основания, кислоты и соли. В эту же классификацию обычно включают и комплексные соединения, поскольку существуют комплексные кислоты, комплексные основания и комплексные соли. Однако уже среди комплексных соединений встречаются такие, которые невозможно отнести ни к одному из перечисленных классов. Таковы, например, карбонилы металлов, многие хелаты и внутрикомплексные соединения. Таким образом, уже применительно к комплексным соединениям приведенная классификация не является полной. Но существуют сложные соединения, которые не относятся и к комплексным, хотя их также нельзя рассматривать в рамках данной классификации. В частности, такие соединения, как CdSnAs2, ZnGePa, CuFeSa и т.п., невозможно отнести к солям, в том числе и комплексным. Причиной неуниверсальности этой классификации служит то, что она охватывает только объекты, в которых существенная роль принадлежит преимущественно ионной связи между структурными элементами. [19]
Термином сложные химические соединения определяют химические индивиды, содержащие три элемента и более. Если простых веществ ( с учетом аллотропии и полиморфизма) насчитывается около 200, а бинарных соединений - порядка 10 000, то сложных химических соединений значительно больше. Традиционно эти объекты подразделяются на три класса: основания, кислоты и соли. В эту же классификацию обычно включают и комплексные соединения, поскольку существуют комплексные кислоты, комплексные основания и комплексные соли. Однако уже среди комплексных соединений встречаются такие, которые невозможно отнести ни к одному из перечисленных классов. Таковы, например, карбонилы металлов, многие хелаты и внутрикомплексные соединения. Таким образом, уже применительно к комплексным соединениям приведенная классификация не является полной. Но существуют сложные соединения, которые не относятся и к комплексным, хотя их также нельзя рассматривать в рамках данной классификации. В частности, такие соединения, как CdSnAs2, ZnGeP2, CuFeS2 и т.п., невозможно отнести к солям, в том числе и комплексным. Причиной неуниверсальности этой классификации служит то, что она охватывает только объекты, в которых существенная роль принадлежит преимущественно ионной связи между структурными элементами. [20]
Курнаков 55 определил бертоллид как химический индивид переменного состава, представляющий собою фазу, не имеющую сингулярных или далътоновских точек на линиях своих свойств. [21]
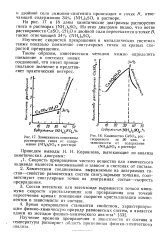 |
Зависимость константы.| Количество CaSO4, растворенного за 50 мин., в зависимости от содержания ( NH4 2SO4 в растворе. [22] |
Скорость превращения чистого вещества или химического индивида является максимальной и зависит в системах от состава. [23]
При наличии всех характерных признаков химических индивидов подобные вещества были лишены особых точек на диаграммах состав - свойство. По мере расширения приложений физико-химического анализа число соединений переменного состава непрерывно увеличивалось. [24]
Во вторую фазу учение о химическом индивиде перешло, когда был поставлен вопрос о природе процесса диссоциации в пределах бертоллидных фаз в свете сложившихся к середине 30 - х годов представлений о валентности и о строении твердых тел. [25]
В химий главными объектами изучения являются химические индивиды. Последние противопоставляются механическим смесям и отличаются от растворов, состоящих из различных химических индивидов. Химический индивид представляет собой фазу, состоящую из одного вида вещества - простого или сложного. [26]
В химии главными объектами изучения являются химические индивиды. Последние противопоставляются механическим смесям и отличаются от растворов, состоящих из различных химических индивидов. Химический индивид представляет собой фазу, состоящую из одною вида вещества, - простого или сложного. [27]
 |
Кубическая структура стехиометрического соединения АВ. а - идеальная структура. б - атом А в междоузлии. [28] |
В химии главными объектами изучения являются химические индивиды. Последние противопоставляются механическим смесям и отличаются от растворов, состоящих из различных химических индивидов. Химический индивид представляет собоц фазу, состоящую из одного вида вещества - простого или сложного. [29]
В идеале понятия чистое вещество и химический индивид совпадают. Это - физически и химически однородное простое тело или химическое соединение, состоящее из одного определенного вида атомов ( ионов) или молекул и обладающее только ему присущим комплексом постоянных свойств. Частицы чистого вещества одинаковы в той мере, в какой это удается установить с помощью современных, очень разнообразных экспериментальных средств. [30]
Страницы: 1 2 3 4