Металлохромный индикатор
Cтраница 2
Все металлохромные индикаторы, кроме хелатообразующих свойств, обязательно обладают и кислотно-основными свойствами. Это объясняется тем, что между процессами образования комплекса с металлом и кислотно-основными изменениями цвета, происходящими за счет диссоциации или протонирования, нет существенной разницы. Чаще всего в обоих процессах участвует фенольный гидроксил, входящий одновременно в группировки, ответственные за хелатообразование и за изменение цвета при изменении рН среды. [16]
Многие металлохромные индикаторы недостаточно устойчивы при хранении в водных растворах, поэтому часто приходится применять только растворы, приготовленные в день работы. Смесь хорошо растирают в ступке и перед титрованием всыпают немного ее в анализируемый раствор. [17]
Большинство металлохромных индикаторов представляет собой органические соединения, которые сами могут образовывать внутри-комплексные соединения с ионами металлов. Цвет внутрикомплексных соединений должен отличаться от цвета свободного индикатора, а его устойчивость должна быть такой, чтобы при титровании комплекс диссоциировал с выделением иона металла при значении рМ, близком к его значению в точке эквивалентности. [18]
Известно много металлохромных индикаторов. [19]
 |
Наиболее распространенные оксред-индикаторы. [20] |
Металлоиндикаторы ( металлохромные индикаторы) используют в комплексометрическом титровании. Это красители, которые образуют с ионами металлов ( М) окрашенные комплексы Mind, менее стойкие, чем комплекс того же металла с ЭДТА. Краситель и его комплекс различаются по окраске. Изменение окраски происходит в тот момент, когда при титровании ЭДТА комплекс индикатора с металлом полностью разрушается, замещаясь более прочным комплексом металла с титрантом, и раствор приобретает окраску свободного индикатора. [21]
Правда, органические металлохромные индикаторы обычно сами довольно сильно окрашены. Поэтому неизбежно растет значение фона, а следовательно, и вероятность флуктуации фона. Чтобы ослабить флуктуации фона, необходимо точно измерять количество вводимого реактива. При соблюдении этих условий определение висмута с металлохромным индикатором значительно более чувствительно, чем определение с иодидом. [22]
Какие из металлохромных индикаторов: а) эриохром черный Т, б) кси-леноловый оранжевый, в) пирокатехиновый фиолетовый - используют при титровании раствором ЭДТА в кислой среде. [23]
При классификации металлохромных индикаторов исходят из типа красителей. В качестве индикаторов применяют азокрасители, трифе-нилметановые красители, гидрохиноны и другие типы соединений. [24]
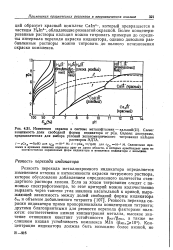
Резкость перехода металлохромного индикатора определяется изменением оттенка и интенсивности окраски титруемого раствора, которое обусловлено добавлением определенного количества стандартного раствора хелона. [26]
Наряду с металлохромными индикаторами для индикации точки эквивалентности применяют также флуоресцентные индикаторы, например флуоресцеинкомплексон [ 59 ( 22) ] или кальцеин W [ 59 - ( ll) j, причем в последнем случае достигают значительного повышения селективности при использовании трена в качестве ти-транта. [27]
Как правило, металлохромные индикаторы интенсивно окрашены, и они образуют ярко окрашенные комплексы с большинством ионов металлов. Более того, комплексы катионов металлов с некоторыми дополнительными комплексующими агентами также отчетливо окрашены. Поэтому для точного обнаружения конечной точки комплексометрического титрования может быть использована спектрофотометрия. Однако, в отличие от визуального определения конечной точки титрования, спектрофотометрический метод часто позволяет следить за изменениями концентрации одной окрашенной частицы даже тогда, когда раствор содержит ощутимые концентрации ряда комплексов, имеющих другие окраски. [28]
Метилтимоловый синий - металлохромный индикатор - можно определить по пику окисления ртути. [29]
Ширина интервала перехода данного металлохромного индикатора и его положение по шкале рН зависит, таким образом, от вида и концентрации иона металла. [30]
Страницы: 1 2 3 4