Восстановление - трехвалентное железо
Cтраница 3
При подготовке раствора, содержащего железо, к титрованию бихроматом или перманганатом калия для восстановления трехвалентного железа до двухвалентного применяют следующие восстановители. [31]
Начертить полученные вольт-амперные кривые и установить области потенциалов, при которых проходят электродные реакции восстановления трехвалентного железа и окисления двухвалентного железа. [32]
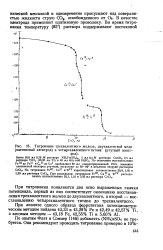 |
Титрование трехвалентного железа, двухвалентной меди ( платиновый электрод и четырехвалентного титана ( ртутный электрод. [33] |
При титровании появляются два ясно выраженных скачка потенциала, первый из них соответствует окончанию восстановления трехвалентного железа до двухвалентного, а второй - восстановлению четырехвалентного титана до трехвалентного. [34]
Особенно большую экономию соляной кислоты дает процесс регенерации хлористого железа и соляной кислоты в результате восстановления образовавшегося трехвалентного железа опять в двухвалентное за счет железа и воды. [35]
На катоде кроме осаждаемого металла выделяется водород или же происходят побочные процессы электрохимического восстановления, например восстановление трехвалентного железа до двухвалентного в ваннах никелирования. [36]
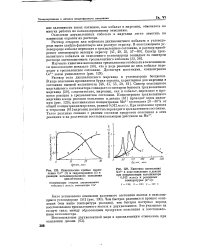 |
Кинетические кривые накопления Со3 ( 1 и гидроперекиси ( 2 в реакции катализированного окисления циклогексана.| Кинетика накопления. [37] |
Чем быстрее развивался процесс окисления ( чем выше температура реакции), тем быстрее наступал период восстановления трехвалентного железа в двухвалентное. Это указывает на тесную связь между образованием продуктов окисления и восстановлением катализатора. [38]
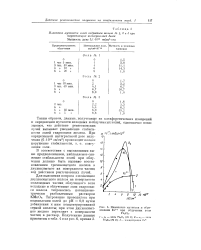 |
Изменение мутности и образование Fe при облучении золя Ге203. [39] |
В соответствии с высказанным выше предположением, наблюдаемое снижение стабильности золой при облучении должно быть вызвано восстановлением трехвалентного железа в двухвалентное на поверхности частиц под действием рентгеновских лучей. [40]
Столь высокое значение константы равновесия показывает, что в рассматриваемой реакции равновесие практически целиком смещено в сторону восстановления трехвалентного железа двухвалентным оловом. При достижении равновесия концентрации ( точнее - активности) ионов Fe3 или Sn2 станут ничтожно малыми по сравнению с концентрациями других ионов. [41]
Сернокислый раствор разбавляют водой до 150 - 175 мл, нагревают до 70 - 80, прибавляют для восстановления трехвалентного железа в двухвалентное1 0 5 г сернокислого гидразина NH2NH2 - H2S04, а при наличии в растворе ванадия и молибдена - 0 1 - 0 2 г щавелевой кислоты. [42]
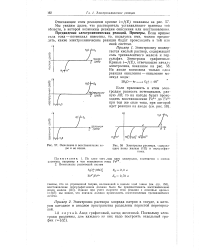 |
Окисление и восстановление воды и ее ионов.| Электролиз раствора, содержащего ионы железа ( III и персульфат-ионы. [43] |
Однако при учете скорости этой реакции с помощью кривых if ( E) мы видим, что сначала должно происходить восстановление трехвалентного железа. [44]
При титровании 0 1 7VCr2SO4 в качестве окислителя применялся 0 1N КМпСч в сернокислом растворе; в этом случае окончанию восстановления трехвалентного железа соответствует более резкий скачок потенциала. При определении титана первые два скачка потенциала в сернокислом растворе более резки, чем в солянокислом растворе, в то время как скачок потенциала по окончании восстановления титана иногда очень неотчетлив. [45]
Страницы: 1 2 3 4