Восстановление - окисное железо
Cтраница 1
Восстановление окисного железа в закисное посредством хлорида двухвалентного олова по описанному методу весьма удобно, т к как производится очень быстро. [1]
Восстановление окисного железа в закисное. Если почва насыщена водой, в ней происходят процессы восстановления железа, приводящие к оглеению почвы. Роль микроорганизмов в восстановлении железа может быть двоякой: 1) восстановление железа может быть результатом накопления восстановленных продуктов ( H2S, H2 и СН4), выделяющихся в процессе брожения, реагирующих с окисным железом; 2) восстановление железа может быть и результатом непосредственного воздействия специфичной группы микроорганизмов на окисное железо, подобно процессу денитрификации, имеющей для них энергетическое значение. [2]
Восстановление окисного железа дает возможность удалить железо из раствора в виде FeSCh 7НаО; кроме того закисное железо легче отмывается от метатитановой кислоты, а окисное железо при промывке метатитановой кислоты образует трудно растворимые основные сульфаты окисного железа. [3]
Для восстановления окисного железа был предложен ряд восстановителей, однако некоторые из них далеко не идеальны. Например, сернистый газ и сероводород хотя и являются эффективными восстановителями, но добавляются в избытке, который затем трудно удалить. Для этого рекомендуется продолжительное кипячение, однако некоторые следы серусодержащих соединений обычно остаются. Рекомендуется также использовать сульфат и хлорид титана ( III), но их растворы неустойчивы и не могут сохраняться продолжительное время. Большого избытка хлорида олова ( II) следует избегать, в противном случае хлорид ртути ( II), добавляемый для удаления избытка хлорида олова ( II), будет восстанавливаться до металлического состояния. [4]
Трудностей, возникающих при восстановлении окисного железа в анализируемом растворе, можно избежать, титруя не за-кисное железо до окисного, а окисное до закисного. Конечную точку определяют по обесцвечиванию красной окраски, которую придает раствору комплекс железа с роданидом. Чтобы определить точку, в которой происходит это изменение, необходимы некоторые навыки, так как вблизи конечной точки реакция протекает довольно медленно. [5]
Общее количество железа определяют после восстановления окисного железа в закисное. [6]
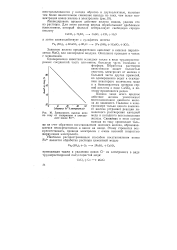 |
Зависимость выхода меди по току от содержания в электролите ионов Fe3. [7] |
Однако чаще всего вредное действие железа уничтожают восстановлением окисного железа до закисного. [8]
По Friedheim y и Nydegger y1 в восстановлении окисного железа нет надобности во всех случах, когда атом железа приходится ка атом или более серы. Далее, по бензидиновому методу пригодные результаты получаются только в том случае, когда на каждую молекулу H2SO4 приходится не более 10 молекул НС1, 15 молекул HNO3, 20 молекул СН3СООН, 5 молекул щелочных солей и 1 - 2 молекул окисного железа. По данным этих авторов при осаждении серной кислоты в виде бензидинсульфата получаются довольно значительные ошибки, компенсирующиеся при соответственных приемах работы. [9]
Определение общего количества железа производят объемным бихроматным методом после восстановления окисного железа в закисное с помощью раствора хлористого олова. В присутствии избытка хлористого олова кремнемолибденовая кислота восстанавливается с образованием молибденовой сини. При обратном титровании бихроматом избытка хлористого олова синяя окраска исчезает, как только заканчивается окисление двухлористого олова, но раньше, чем начнет окисляться закисное железо. [10]
Исходя из этого различия между двумя основаниями Кун и Вас-серман пришли к выводу, что восстановление окисного железа в закисное не может быть лимитирующей стадией процесса образования комплекса. Они предположили, что после образования этим путем ионов закисного железа последние могут либо окисляться перекисью, либо реагировать с основанием, образуя комплекс. [11]
Таким образом, выделение кислорода фактически определялось измерением скорости образования оксигемогло-бина в анаэробных смесях хлоропластов с оксалатом окисного железа и гемоглобином ] восстановление окисного железа определялось измерением скорости в аэробных смесях хлоропластов с оксалатом окисного железа и метгемоглобином. [12]
В природных условиях в заболоченных почвах протекают физико-химические процессы без достаточного доступа атмосферного воздуха, следовательно, бактериальные процессы идут за счет восстановления окисного железа и других солей, которые находятся в заболоченных почвогрунтах востановленными до закис-ной формы. Закись железа представляет собой легкорастворимую соль, дающую при доступе воздуха гидроокись железа. Соединения гидроокисей находятся в почвогрунте в виде коллоидных растворов, препятствующих передвижению воды при фильтрации. Кроме того, заболоченные грунты в большинстве случаев содержат большое количество пылеватых ( от 0 05 до 0 005 мм) фракций, и при наличии в содержании грунта закисных форм железа эти грунты обладают очень плохой фильтрацией. Как известно, оглеенные грунты способны при увлажнении сильно набухать, удерживать большое количество воды и при переувлажнении переходить в текучее состояние. [13]
Еще до полного растворения всех сульфатов в бак / 5 загружают мелкие железные стружки в количестве несколько меньшем, чем требуется по расчету для восстановления окисного железа в закисное. Заканчивают восстановление, опуская в бак 18 корзину 24 с железными стружками. Корзина 24 поднимается талью и передвигается по монорельсу. Установив анализом, что в растворе имеется ТГ - 3 г / л в пересчете на ТЮч восстановление заканчивают, корзину 24 вынимают из бака 18 и ополаскивают ее в баке 25, содержащем слабую кислоту, чтобы предупредить гидролиз раствора, оставшегося на стружках. [14]
При ог-леении он наиболее проявляется в условиях ослабленного выноса продуктов глеевого процесса и почти не отмечается при хорошо выраженных нисходящих токах воды при кислой реакции почвенных растворов. Наиболее характерная сссбенносгь глееобразования - восстановление окисного железа в закисное. Оно может происходить, по-видимому, в результате как ферментативной деятельности микроорганизмов, так и воздействия продуктов жизнедеятельности анаэробных микроорганизмов. К таким продуктам могут относиться газообразные соединения ( Н2, H2S), низкомолекулярные органические кислоты и гуминовые кислоты. [15]
Страницы: 1 2