Восстановление - ион - водород
Cтраница 3
Это означает, что существует связь между задержкой восстановления ионов водорода и способностью металла катализировать реакцию рекомбинации водородных атомов. [31]
В качестве примера рассмотрим более подробно кинетику процесса восстановления иона водорода ( гл. [32]
 |
Схема развития процесса подшламовой коррозии. [33] |
При значениях показателя рН7 скорость коррозии определяется скоростью восстановления ионов водорода. [34]
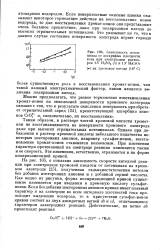 |
Зависимость потенциала от логарифма плотности тока при электролизе растворов IN H2SO4 ( о и IN HaCrO. [35] |
Если поверхностные окисные пленки оказывают некоторое тормозящее действие на восстановление ионов водорода, то для восстановления хромат-ионов они представляют очень большое препятствие, даже при поляризации катода до высоких отрицательных потенциалов. [36]
 |
Схема развития пр. [37] |
При значениях показателя рН7 0 скорость коррозии определяется скоростью восстановления ионов водорода. Ионы водорода, имеющиеся в котловой воде, из-за ее диссоциации или кислотного характера примесей восстанавливаются до водорода ( на катодных участках) и растворяются в металле. Происходят интенсивная коррозия и насыщение водородом металла. [38]
Эти катодные реакции основаны, таким образом, на восстановлении ионов водорода. [39]
Уменьшение содержания карбидов при повышении температуры закалки тормозит катодный процесс восстановления ионов водорода. Оба фактора приводят к уменьшению коррозии стали. Образование металлической пленки на поверхности стали можно объяснить избирательной коррозией б-феррита - на поверхности остается рыхлый слой, обедненный ферритом. [40]
Принятые сокращения: a - диффузионный ток маскируется вовраста-нием тока вследствие восстановления иона водорода или натрия; Ь - не восстанавливается; с - отсутствует четко выраженный предельный ток; d - диффузионный ток плохо выражен и пропорциональность между величиной диффузионного тока н концентрацией отсутствует. [41]
 |
Изменение поляризационных кривых при реакции нейтрализации.| Изменение поляризационных кривых при реакции осаждения. [42] |
Обе реакции приводят к одинаковому результату и весь ток расходуется на восстановление ионов водорода. [43]
С другой стороны, сдвиг компромиссного потенциала в положительную сторону тормозит восстановление ионов водорода ( или воды) на обоих металлах. Общее количество выделившегося водорода может расти или уменьшаться во времени в зависимости от величиг ны разности ащ и ан2, скорости увеличения площади электроположительного металла и величины смещения компромиссней. [44]
Высокое водородное перенапряжение давно обратило на себя внимание ученых и реакция восстановления ионов водорода на катоде стала предметом весьма многочисленных и тонких исследований. Современные представления об электрохимической кинетике сложились, в значительной степени, именно при изучении этой реакции. Восстановление водорода на таких катодах, где перенапряжение достаточно велико, позволяет наблюдать основные закономерности электрохимической кинетики, не затемненные побочными явлениями. [45]
Страницы: 1 2 3 4