Восстановление - кадмий
Cтраница 2
 |
Степень адсорбции гомологического ряда ПАВ второй группы в зависимости от их молекулярного веса. [16] |
Как видно из графика, исследованная добавка вызывает некоторое снижение предельного тока восстановления кадмия. Аналогичный эффект достигается и в результате введения в электролит добавок № 8, № 11 и др. Добавки первой группы в исследованных условиях практически не влияют на полярограмму кадмия. [17]
Например на рис. 7.32, б показаны активная и реактивная составляющие тока для восстановления кадмия и получены ожидаемые соотношения угла сдвига фаз. Реактивная составляющая на рисунке содержит существенный вклад тока заряжения, как это имеет место в полярографии. Следовательно, фазочувствительное определение также обеспечивает значительное усовершенствование метода переменнотоковой вольтамперометрии. [18]
Освободившиеся ионы кадмия титруют раствором ферроцианида калия ( см. раздел Кадмий) по току восстановления кадмия на ртутном капельном электроде; в качестве анода был применен ртутный донный электрод. [19]
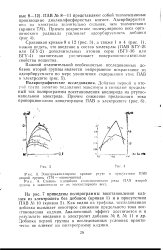
На рис. 5.23 приведены вольтамперограммы с линейной разверткой потенциала - нормальная и первая производная - для восстановления кадмия. Видно, что на производной кривой очень острые пики, а это значит, что характерной особенностью этого метода является, очевидно, улучшенная разрешающая способность. Рисунок демонстрирует также высокую воспроизводимость, которая достигается при регистрации производной: обе кривые на нем зарегистрированы трижды, и они почти полностью совпадают. [21]
 |
Кривые анодной поляризации кадмия в электролитах. [22] |
Добавка сернистого натрия ( 35 г / л) делает более устойчивым состав электролита, хотя практического влияния на процесс восстановления кадмия не оказывает. Сернокислый никель в цианистом электролите необходим для повышения блеска покрытия. [23]
При потенциале электрокапиллярного нуля на поверхности ртутной капли исчезает градиент поверхностного натяжения и максимум не появляется, как например в случае восстановления кадмия. [24]
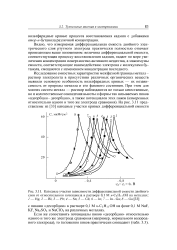 |
Катодные участки зависимости дифференциальной емкости двойного слоя от относительного потенциала в растворе 0 1 М н - CsHnOH на металлах. [25] |
Видно, что измеряемая дифференциальная емкость двойного электрического слоя ртутного электрода практически полностью отвечает приведенным выше положениям: величина дифференциальной емкости, соответствующая процессу восстановления кадмия, падает по мере увеличения концентрации поверхностно-активного вещества, а максимумы емкости, соответствующие взаимодействию электрона с молекулами бу-танола, смещаются с изменением концентрации последнего. [26]
Сперва осаждают никель титрованным раствором диметилглиоксима, проверяя полноту осаждения; диметил-глиоксим должен быть взят в избытке; затем, не отфильтровывая осадок, титруют кадмий комплексоном III по току восстановления кадмия на ртутном капельном электроде при - 1 2 в ( Нас. Когда титрование кадмия закончено, добавляют в раствор несколько капель раствора соли кадмия для того, чтобы избыток комплек-сона не мог связываться с никелем, солью которого титруют избыток диметилглиоксима. [27]
Сначала осаждают никель титрованным раствором диметилглиоксима, проверяя полноту осаждения ( диметилглиоксим должен быть взят в избытке), затем, не отфильтровывая осадок, титруют кадмий раствором ЭДТА по току восстановления кадмия на ртутном капающем электроде при - 1 2 В ( Нас. Когда титрование кадмия закончено, добавляют в раствор несколько капель раствора соли кадмия для того, чтобы избыток ЭДТА не мог связываться с никелем, солью которого титруют избыток диметилглиоксима. Описанный метод был применен для анализа массы щелочных аккумуляторов при соотношении никеля и кадмия 1: 30, а также для анализа ванн, используемых для приготовления пластин аккумуляторов. [28]
Хотя возможность восстановления водородом FeS, присутствующего в концентрате, до сих пор нами, не обсуждалась, однако можно легко показать, что равновесное отношение H2S / H2, устанавливающееся при восстановлении кадмия и цинка, настолько больше, чем отношение Н28 / Н3 в равновесии с FeS, что это вещество не может быть восстановлено до тех пор, пока CdS не будет предварительно удален из равновесной системы. [29]
Кадмий ( Cd2) обратимо восстанавливается в растворе KNOS. Восстановление кадмия начинается при потенциале более отрицательном, чем потенциал восстановления кислорода. Поэтому при определении кадмия необходимо удалять из раствора кислород. [30]
Страницы: 1 2 3 4