Восстановление - кетогруппа
Cтраница 2
Ретросинтетический анализ алкиларенов предусматривает разъединение боковой цепи и ароматического ядра, что соответствует реакции алкилирования или ацетилирования с последующим, восстановлением кетогруппы. [16]
Выше уже приводились примеры ацетатных и преимущественно ароматизированных поликетидных антибиотиков из стрептомицетов [ например, ( 108) и ( 129) ]; еще более велико разнообразие структур соединений, для которых типичной является промежуточная степень восстановления кетогрупп ( частично до по-лиолов, а частично - до полиенов) ( см. разд. [17]
Примечательно, что на всех стадиях использовались очень простые и давно известные реакции: кротоновая конденсация - j - реакция Михаэля ( 68 69 - f 68 - 70), расщепление двойной связи через стадию гидроксилирования ( получение 72), ацилирование кетонов по а-углеродному атому ( 72 - - 7; ) и, наконец, восстановление кетогрупп и дегидратация. [18]
Восстановление циклических кетонов осуществляется с высокой степенью стереоселективности. При восстановлении кетогруппы сложных полициклических систем стереоселективность реакции зависит от пространственной доступности кетогруппы: действие алюмогидрида лития на сте-рически незатрудненные кетоны приводит к образованию преимущественно спиртов с экваториальной гидроксильной группой, а из стерически затрудненных кетонов в этой реакции образуются главным образом спирты с аксиальным положением гидроксила. [19]
Ключевой стадией синтеза является получение кетосахара, что достигается обычно окислением соответствующим образом защищенного моносахарида хромовым ангидридом в пиридине ( см. гл. В настоящее время, после открытия гораздо более эффективного и специфичного окислителя - четырехокиси рутения 47 и нового способа восстановления кетогруппы в дезоксизвено действием на арилсульфонилгидразоны бор-гидридов щелочных металлов 48, такой путь выглядит особенно многообещающим для синтеза разнообразных дезоксисахаров. [20]
Общий характер тиофенового метода иллюстрируют синтезы ди-гидрогиднокарповой, дигидрохаульмугровой кислот и циклогексилпро-изводного С6Нп ( СН2) юСООН - С помощью этого общего метода Миллер ( 1959, 1961) синтезировал ряд 10-оксикислот с длинной цепью. Например, кислота н - СуН СНаЬСЩОН) ( СН2) 8СООН была получена последовательно конденсацией 2-н-гептилтиофена с хлорангидридом 9-карбэтоксипеларгоновой кислоты, восстановлением кетогруппы бор-гидридом натрия, гидролизом и десульфированием. [21]
K - C7Hi5 ( CI - l2) 4CH ( OH) ( GH2) 8COOH была получена последовательно конденсацией 2-н-гептилтиофена с хлорангидридом 9-карбэтоксипеларгоновой кислоты, восстановлением кетогруппы бор-гидридом натрия, гидролизом и десульфированием. [22]
Для выяснения вопроса о том, является ли подобное аномальное протекание реакции общим для f - кетокислот с другими циклами ароматического характера И. М. Липович и С. И. Сергиевской были подвергнуты восстановлению с помощью сплава Ni - А1 аналогичные кислоты ряда нафталина и бензола, причем во всех случаях ими также наблюдалось образование соответствующих оксикислот. Таким образом, очевидно, что наличие карбоксильной группы оказывает тормозящее действие при восстановлении у-алкоксиарилкетокислот сплавом Ni - А1; это выражается в получении в качестве конечных продуктов не кислот, которые должны были образоваться при восстановлении кетогруппы в ме-тиленовую, а оксикислот, что может произойти лишь при восстановлении карбонильной группы до вторично-спиртовой. [23]
Этот метод состоит из комбинации хорошо разработанных реакций. Хлорангидрид кислоты превращают в диазокетон, который при действии ледяной уксусной кислоты дает ацетоксикетон. В результате восстановления кетогруппы и одновременно происходящего гидролиза получают соответствующий гликоль. При окислительном расщеплении гликоля образуется альдегид, который содержит такое же количество атомов углерода, что и исходные вещества, а именно кислота или ее хлорангидрид. [24]
С точки зрения использования в качестве лекарственных препаратов, диацетиленовые и ениновые производные представляют несомненный интерес и реальную основу, так как многие из подобных препаратов могут быть синтезированы на основе диаце-тилена. Показано [274], что различного рода биологическая активность изменяется и часто исчезает совсем при незначительных изменениях структуры ацетиленового соединения. Так, обнаружено, что восстановление кетогруппы или уменьшение числа ацетиленовых связей в молекуле капиллина приводит к резкому ослаблению антимикробных свойств этого соединения, благодаря чему все производные капиллина значительно активнее аналогичных соединений капиллена, что свидетельствует о том, что в данном случае, именно группировка С 6H6COCCCsG - обеспечивает антимикробную активность. [25]
С точки зрения использования в качестве лекарственных препаратов, диацетиленовые и ениновые производные представляют несомненный интерес и реальную основу, так как многие из подобных препаратов могут быть синтезированы на основе диаце-тилена. Показано [274], что различного рода биологическая активность изменяется и часто исчезает совсем при незначительных изменениях структуры ацетиленового соединения. Так, обнаружено, что восстановление кетогруппы или уменьшение числа ацетиленовых связей в молекуле капиллина приводит к резкому ослаблению антимикробных свойств этого соединения, благодаря чему все производные капиллина значительно активнее аналогичных соединений капиллена, что свидетельствует о том, что в данном случае именно группировка С 6Н5СОССС С - обеспечивает антимикробную активность. [26]
 |
Антибиотики, синтезируемые различными штаммами Streptomyces, в том числе штаммами, трансформированными плазмидами рШЗОЗ и PIJ23151. [27] |
Поликетидные антибиотики синтезируются по тому же пути, что и длинноцепочечные жирные кислоты. В результате каждого цикла конденсации к растущей углеродной цепи добавляется р-кетогруппа. Процесс состоит из ряда повторяющихся стадий, включающих восстановление кетогруппы, дегидратацию и восстановление р-еноильных групп в растущей полике-тидной цепи. Второй класс включает синтазы, образованные несколькими полипептидами ( А - Е на рис. 12.13, Б); каждый из них имеет свой активный центр и обладает специфической ферментативной активностью, катализирующей определенную реакцию биосинтеза. [28]
Исходным соединением в первом полном синтезе морфина послужил диметокси-о-нафтохинон ( 7), полученный в свою очередь по 10-стадийной схеме из 2 6-дигидро-ксинафталина Реакцией Михаэля с циакуксусным эфиром и дальнейшими превращениями хинон ( 1) был переведен в цианметкльное производное ( 2), к которому диеновым синтезом был достроен третий карбоцикл молекулы алкалоида. Частичное гидрирование полученного цианоднкетона U) сопровождалось циклизацией, но в образовавшемся кетолактаме ( 4) гетероцикл и второй карбоцикл молекулы имели нежелательное yuc - сочленение. При монобромировании и дегидробромировании последнего с одновременным образованием фенилгндразона происходила необходимая изомеризация в транс - сочлененное соединение ( 7), которое затем было вновь переведено в кето-проиэводное ( в), имеющее уже нужную стереохимию. Превращение его в кодеин легко протекало при трибромированнн, замыкании пятого ( дигидрофуранового) кольца и восстановлении кетогруппы с одновременным восстановительным дебро-мироваинем; морфин образовывался при деметилированни кодеина хлоргидратом пиридина. [29]
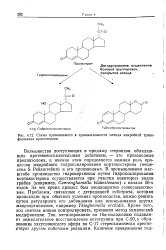 |
Схема применяемого в промышленности метода микробной трансформации прогестерона. [30] |
Страницы: 1 2 3