Восстановление - комплекс - металл
Cтраница 1
Восстановление комплексов металлов часто проводят на ртутном катоде, в частности в полярографии - на ртутном капельном электроде. При этом вместо катодно-анодной волны, которой отвечают два предельных диффузионных тока - катодный и анодный, наблюдается одна катодная волна, характеризующаяся одним предельным током - катодным. [1]
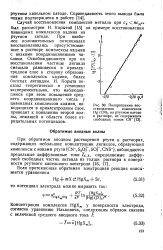 |
Полярограмма восстановления комплексов Hg ( CN3 на ртутном катоде в растворе, не содержащем свободных ионов CN -. [2] |
Случай восстановления комплексов металла при сх - ncnz был рассмотрен И. [3]
Кинетические токи часто наблюдаются и при восстановлении комплексов металлов, если в растворе находятся в равновесии несколько комплексов одного и того же иона металла, различающихся числом лигандов, при условии, что восстановление этих комплексов происходит при различных потенциалах. [4]
Им предложены уравнения, описывающие обратимые подярограммы восстановления комплексов металлов в случае индуцированной лигандами адсорбции комплексов металлов, когда последние адсорбируются на занятых адсорбированными лигандами участках поверхности электрода, и при адсорбции комплексов на участках, свободных от адсорбированных лигандов. [5]
Подробный анализ полярографических волн, наблюдаемых при восстановлении комплексов металлов в случае медленного протекания предшествующей диссоциации комплексов, был проведен И. [6]
При рН2 6 протекает одна четырехэлектронная необратимая реакция. В присутствии Ni появляется пик, обусловленный восстановлением комплекса металла. [7]
Особо прочные комплексы при соответствующих условиях восстанавливаются непосредственно при практически полном отсутствии или лишь частичной диссоциации. При этом действуют особые закономерности. Восстановление комплексов металлов, образующих амальгамы, протекает, как правило, обратимо. [8]
Замещение, катализируемое комплексами палладия и никеля. Катализ реакций арилгалогенидов и арилтрифлатов комплексами палладия и никеля предоставляет, большие возможности для введения алкильных, алкенильных и алкинильных групп в ароматическое кольцо. Лигандами в комплексе служат чаще всего молекулы трифенил-фосфина, являющегося сильным о-электронодонором, который повышает электронную плотность на атоме металла и увели ш-еает активность и стабильность катализатора. Координационно ненасыщенный комплекс Pd или Ni генерируется в реакционной среде в результате восстановления комплекса металла ( II) или диссоциации координационно насыщенного комплекса металла. [9]
Не удивительно поэтому, что аналогичное изменение претерпевают и полярографические потенциалы полуволн. Данные, приведенные в табл. 21 - 1, показывают, что потенциал полуволны восстановления комплекса металла обычно более отрицателен, чем потенциал полуволны реакции восстановления соответствующего простого иона. [10]
В книге рассматриваются электродные процессы, протекающие с участием комплексов металлов в условиях равновесия и при наличии внешнего поляризующего тока. Описаны основные электрохимические методы, используемые при определении состава и констант устойчивости одноядерных комплексов металлов. Рассматривается кинетика электродных процессов, протекающих с участием комплексов металлов в условиях диффузионного контроля, при медленном протекании электрохимической стадии и при наличии медленных предшествующих химических реакций в растворе. Обсуждается механизм стадий разряда и ионизации, в которых участвуют комплексы металлов, а также влияние строения двойного электрического слоя на скорости реакций восстановления комплексов металлов. Одна из глав посвящена стационарным и нестационарным методам исследования кинетики электродных процессов. [11]
Страницы: 1