Восстановление - металл
Cтраница 2
Восстановление металлов из их соединений другими металлами, химически более активными, называется металлотермией. Эти процессы протекают также при повышенных температурах. [16]
Восстановление металлов сопровождается значительной затратой энергии ( см. табл. 55), которая может быть передана восстанавливающемуся металлу различными способами. [17]
Восстановление металлов из их соединений другими металлами, химически более активными, называется металлотермией. Эти процессы протекают также при повышенных температурах. В качестве восстановителей применяют алюминий, магний, кальций, натрий, а также кремний. Если восстановителем является алюминий, то процесс называется алюминотермией, если магний - магнийтермией. [18]
Восстановление металлов из оксидов с помощью алюминия называется алюмотермией. Особое значение этот метод имеет для получения тугоплавких металлов: хрома, ванадия, марганца и др. Алюмотермию используют также при сваривании металлических деталей и рельсов. [19]
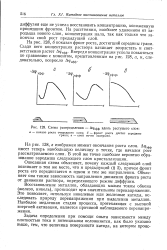 |
Схема распределения - Дфзфф вдоль растущего слоя. [20] |
Восстановление металлов, обладающих малым током обмена ( железо, никель), происходит при значительном перенапряжении. Это позволяет, используя никелевые или железные катоды, исследовать природу перенапряжения при выделении металлов. Наиболее медленная стадия процесса, протекающая с высокой энергией активации, является причиной наблюдаемого перенапряжения. [21]
Восстановление металлов, обладающих малым током обмена ( железо никель), происходит при значительном перенапряжении. Это позволяет, используя никелевые или железные катоды, исследовать природу перенапряжения при выделении металлов. Наиболее медленная стадия процесса, протекающая с высокой энергией активации, является причиной наблюдаемого перенапряжения. [22]
Восстановление металлов из их окислов и солей, предварительно измельченных и высушенных в печах проходного типа в присутствии твердого углерода - сажи, водорода, газообразных углеродистых или углеродоводородных соединений. [23]
Восстановление металлов из оксидов или хлоридов осуществляют в водородной плазме. Полученный плазменным восстановлением порошок вольфрама можно применять для производства твердых сплавов. [24]
Восстановление металлов в пирометаллургических способах осуществляется, главным образом, при помощи кокса и окиси углерода, получаемой из кокса непосредственно в печи при неполном сгорании углерода. Часть кокса, при получении чугуна в домне, заменяют природным, коксовым газом. Образующиеся примеси отделяются от основного металла путем их ошлаковывания в виде окислов и солей, главным образом, в виде легкоплавких силикатов. [25]
Восстановление металлов из руд - производится не только теплом, выделяющимся при сгорании топлива, но и образующимся из электрической энергии. Согласно закону Джоуля 1 квт-ч эквивалентен 860 ккал тепла. [26]
Восстановление металлов из их оксидов можно осуществлять и с помощью других простых веществ, имеющих более высокое сродство к кислороду ( кремний; алюминий), благодаря чему такие реакции сопровождаются выделением большого количества тепла и называются злементотермическими. [27]
Восстановление металлов из их соединений другими металлами, химически более активными, называются м е т а л л о т е р м и-е и. Эти процессы протекают также при высоких температурах. В качестве восстановителей используют алюминий, магний, кальций, натрий, а также кремний. Если восстановителем является алюминий, то процесс называется алюминотермией, если магний - магнийтермией. [28]
Восстановление металла водородом имеет много общего с восстановлением его окисью углерода. Однако водород слабее, чем СО, раскисляет металл. [29]
Восстановление металлов из окислов водородом-гетерогенный равновесный процесс. При некоторой данной температуре в газовой фазе всегда имеется определенное соотношение между количеством водорода и количеством паров воды. Присутствие водорода в газовой фазе указывает на то, что он как восстановитель слабее таких сильных восстановителей, как алюминий, магний и др., окислы которых имеют большие теплоты образования и небольшое давление диссоциации по сравнению с парами воды. Но водород как восстановитель все же выгодно отличается от указанных металлов тем, что реакции с ним являются гетерогенными и что в этом случае пары воды можно легко удалить из реакционного пространства, сместив тем самым равновесие в сторону получения металла. [30]
Страницы: 1 2 3 4