Восстановление - никель
Cтраница 2
В случае восстановления никеля ВН4 - - или Н2РО2 - - ионами кристаллическая фаза покрытия при малом содержании Р или В представляет собой метастабильный пересыщенный твердый раствор внедрения бора ( или замещения фосфором) в гцк-ре-шетке никеля. [16]
Для процессов восстановления никеля, например, характерны повышенные температуры ( почти до 100 С в кислых растворах), а для процесса химического восстановления меди формальдегидом - температуры 20 - 50 С, причем выбор температурного режима определяется природой лиганда. Химическое меднение в тартратных растворах проводят обычно при температуре от 18 до 30 С, а в растворах на основе ЭДТА - при температуре выше 40 С. Стабильность растворов химического меднения с повышением температуры снижается, поэтому в растворах, работающих при повышенных температурах, всегда содержатся стабилизирующие добавки, которые позволяют получать осадки хорошего качества даже при температурах, более 70 СС. [17]
Для процессов восстановления никеля, например, характерны повышенные температуры ( почти до 100 С в кислых растворах), а для процесса химического восстановления меди формальдегидом - температуры 20 - 50 С, причем выбор температурного режима определяется природой лиганда. Химическое меднение в тартратных растворах проводят обычно при температуре от 18 до 30 С, а в растворах на основе ЭДТА - при температуре выше 40 С. Стабильность растворов химического меднения с повышением температуры снижается, поэтому в растворах, работающих при повышенных температурах, всегда содержатся стабилизирующие добавки, которые позволяют получать осадки хорошего качества даже при температурах, более 70 С. [18]
Скорость процесса восстановления никеля зависит прежде всего от температуры и кислотности раствора. При низкой температуре процесс практически не идет. Температура раствора должна быть от 80 до 98 С. [19]
О механизме восстановления никеля с помощью гипофосфита высказано несколько гипотез. Наибольшим признанием пользовалось представление, согласно которому восстановление никеля происходит посредством атомарного водорода, выделяющегося в результате взаимодействия гипофосфита натрия с водой. [20]
Одновременно с восстановлением никеля протекает реакция восстановления гипофосфита до элементарного фосфора. Реакция, приводящая к образованию фосфора, связана с разрывом связей Р - Н, Р - О и Р - ОН в молекуле гипофосфита. [21]
Но при восстановлении никеля образуются очень мелкие кристаллы. Поверхность такого мелкокристаллического осадка представляет в среднем, если электрод не чрезмерно мал, постоянную величину. Вследствие этого можно считать, что кажущаяся плотность тока пропорциональна истинной плотности. [22]
Чем медленнее протекает восстановление никеля, тем более активным он становится. Водород не является необходимым для восстановления формиага никеля, но служит для удаления паров воды. [23]
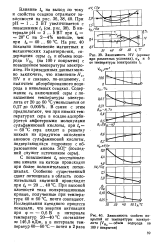 |
Зависимость свойств покрытий от температуры электролита ( VHj - объем водорода на 100 г покрытия. [24] |
С повышением ta восстановление никеля на катоде происходит при более положительных потенциалах. При высокой плотности тока поляризационные кривые, полученные при температуре 40 и 60 С, почти совпадают. [25]
Первая стадия отвечает восстановлению никеля из комплекса и лимитируется диффузией, вторая соответствует восстановлению протонированных лигандов в составе комплекса и лимитируется кинетикой реакции протонирования. [26]
Первая стадия отвечает восстановлению никеля из комплекса и лимитируется диффузией, вторая соответствует восстановлению протонированных лигандов в составе комплекса и лимитируется кинетикой реакции протонйрования. [27]
Вторая волна обусловлена восстановлением гидратированного никеля ( II) и может быть устранена, если сделать достаточно большой концентрацию хлорида. [28]
Органические добавки ускоряют процесс восстановления никеля; некоторые из них связывают ионы никеля в комплексное соединение, предупреждая выпадение фосфитов никеля. Скорость восстановления никеля возрастает до максимума с увеличением концентрации добавок, при - этом осаждаются гладкие, блестящие осадки. При дальнейшем повышении концентрации органических соединений скорость осаждения никеля падает, качество осадков ухудшается. [29]
При снижении рН скорость восстановления никеля заметно падает, при рН6 0 из раствора выпадают малорастворимые соединения - фосфиты никеля, ухудшающие качество осадка. Для поддержания постоянного значения рН в раствор вводят буферирую-щие добавки: натриевые соли лимонной, уксусной и янтарной кислот, молочную и аминоуксусную кислоты и др. Некоторые из них, например: аминоуксусная кислота, лимоннокислый натрий образуют с никелем комплексные соединения, вследствие чего повышается устойчивость раствора и увеличивается продолжительность его работы. [30]
Страницы: 1 2 3 4