Восстановление - бихромат - калий
Cтраница 1
Восстановление бихромата калия углем может быть совмещено с получением бихромата калия поташным способом ( стр. [1]
 |
Кинетика восстановления бихромата калия сульфитом натрия ( рН 4. [2] |
Кинетика восстановления бихромата калия сульфитом натрия при рН 4 приведена на рис. 8.6 ( см. Гордин И. В. и др. Оптимизация химико-технологических систем очистки промстоков. [3]
Реакция восстановления бихромата калия древесным углем протекает с большим выделением тепла. Лабораторными опытами было установлено, что температура воспламенения смеси бихромата калия с древесным углем зависит от содержания в ней древесного угля. В ходе реакции температура спека поднимается до 1100 благодаря чему процесс восстановления протекает очень быстро и заканчивается почти полностью вместе с окончанием процесса горения угля. Этот процесс восстановления сопровождается образованием жидкой фазы, состоящей, вначале, из эвтектической смеси хромата калия с бихроматом калия, а затем с карбонатом калия. Наличие жидкой фазы приводит к спеканию массы с образованием пористого спека. Горячий спек очень непрочен и легко ломается, при охлаждении до - 20 прочность спека резко возрастает. От соприкосновения горячего спека с воздухом происходит обратное окисление окиси хрома, с образованием хромата калия. [4]
Высокая степень восстановления бихромата калия, достигаемая при обжиге шихты в цепной печи, позволяет значительно упростить технологическую схему производства побочного продукта-карбоната калия-путем очистки его от незначительных количеств шестивалентного хрома непосредственно в стадии горячего выщелачивания спека. [5]
Вместо серы для восстановления бихромата калия можно использовать крахмал или углерод. [6]
Производство окиси хрома путем восстановления бихромата калия древесным углем до последнего времени осуществлялось периодически сжиганием ( с помощью запала) шихты в сталвных тиглях. Полученный спек после охлаждения смачивали, выдерживали для размягчения и затем выгружали из тиглей в бак с мешалкой, где он выщелачивался при подогреве острым паром. [7]
Получают их обычно путем восстановления бихромата калия в присутствии необходимого количества серной кислоты. [8]
 |
Стандартная шкала для определения диэтилового эфира. [9] |
Метод основан на реакции восстановления бихромата калия в сернокислой среде, сопровождающейся изменением окраски раствора. [10]
Ионы хрома, образующиеся при восстановлении бихромата калия, окрашены в зеленый цвет. В точке эквивалентности происходит переход окраски от синей ( иод-крахмальная реакция) до зеленой. Этот пег реход в концентрированных растворах солей хрома; воспринимается плохо. Чтобы облегчить наблюдение точки эквивалентности, целесообразно разбавить раствор перед титрованием дистиллированной водой. [11]
Термический твердофазный способ основан на восстановлении бихромата калия серой. [12]
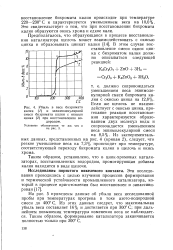 |
Убыль в весе бихромата калия ( / и эквимолекулярной смеси бихромата калия с окисью цинка ( 2 при восстановлении водородом. [13] |
Это свидетельствует о том, что при восстановлении бихромата калия образуются окись хрома и едкое кали. [14]
Для высокопроизводительной работы цепной печи необходимо, чтобы реакция восстановления бихромата калия протекала с интенсивным выделением пламени. Этому требованию удовлетворяет шихта, содержащая не менее 9 % древесного угля. [15]
Страницы: 1 2