Восстановление - висмут
Cтраница 1
Восстановление висмута из его окиси Bi203 п других окислон висмута проводят при 380 - 400 С ( см. также стр. [1]
Восстановление висмута в растворе НС1 полностью обратимое. [2]
Восстановление висмута из его окиси Bi2O3 и других окислов висмута проводят при температуре 380 - - 400 ( см. также стр. [3]
Относительно восстановления висмута свинцом в литературе имеются1 противоречивые данные. [4]
В кислых растворах восстановление висмута начинается при потенциалах, близких к потенциалам восстановления меди. [5]
На реакциях окисления - восстановления висмута основано большое число ценных аналитических методов открытия и определения висмута. [6]
Пршибил и Матыска титруют висмут комплексоном III, используя восстановление висмута на ртутном капельном электроде. При рН, равном 1 - 2, комплексонаты других металлов не образуются, поэтому добавляемый при титровании комплексен связывается только с висмутом, по току которого проводится титрование [ при потенциале около - 0 18 в ( Нас. Мешать этому определению могут ионы, восстанавливающиеся при том же потенциале - сурьма, железо, олово; их связывают в лимонно - или виннокислый комплекс, сдвигая потенциал их восстановления в более отрицательную область. [7]
Пршибил и Матыска титруют висмут комплексоном III, используя восстановление висмута на ртутном капельном электроде. При рН, равном 1 - 2, комплексонаты других металлов не образуются, поэтому добавляемый при титровании комплексен связывается только с висмутоти, по току которого проводится титрование [ при потенциале около - 0 18 в ( Нас. Мешать этому определению могут ионы, восстанавливающиеся при том же потенциале - сурьма, железо, олово; их связывают в лимонно - или виннокислый комплекс, сдвигая потенциал их восстановления в более отрицательную область. [8]
Пршибил и Матыска титруют висмут ( III) раствором ЭДТА, используя восстановление висмута ( III) на ртутном капающем электроде. При рН1 - 2 комплексонаты других металлов не образуются, поэтому добавляемый при титровании ЭДТА связывается только с висмутом, по току которого проводят титрование при потенциале около - 0 18 В ( Нас. [9]
Полезной иллюстрацией квазиобратимого переменнотокового электродного процесса с обратимым постояннотоковым переносом заряда может служить восстановление висмута ( Ш) [ BirlI 3e Bi ( Hg) ] в хлорной кислоте в присутствии изменяющейся концентрации хлорида. [10]
Висмут восстанавливается на платиновом электроде, поэтому описанное титрование можно проводить и по току восстановления висмута без наложения внешнего напряжения. [11]
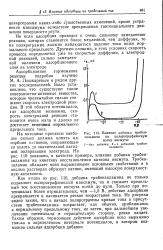 |
Влияние добавки трибензиламина на полярографическую волну висмута. [12] |
Как видно из рис. ПО, добавка трибензиламина не только подавляет полярографический максимум, но и снижает предельный ток восстановления висмута почти до нуля. Только при потенциалах более отрицательных, чем - 1 5 В, действие адсорбции прекращается и начинается резкое возрастание тока. Из рисунка видно также, что в начале подпрограммы кривая тока в присутствии трибензиламина возрастает, как обычно, приближаясь к нормальному предельному току, но затем, при дальнейшем увеличении потенциала в отрицательную сторону, резко падает. Таким образом, тормозящее действие адсорбции ясно выражено только в определенном интервале потенциалов, в котором возможна сильная адсорбция добавки. [13]
Если в растворе отсутствуют катионы сурьмы и ртути ( И), то висмут ( Ш) открывают реакцией восстановления висмута ( Ш) до металлического висмута оловом ( И) ( точнее - комплексами [ Sn ( OH) 4 ] -) - наблюдается образование черного осадка, содержащего металлический висмут. [14]
При 0 005 % желатины волны для всех четырех элементов выражены хорошо, но при 0 01 % желатины волна висмута ставовится более пологой, а горизонтальная площадка на кривой после восстановления висмута и до начала восстановления свинца отсутствует. При 0 03 % желатины волна висмута совсем исчезает, а для свинца и кадмия диффузионные токи сильно уменьшаются. [15]
Страницы: 1 2