Восстановление - водород
Cтраница 1
Восстановление водорода [ ( уравнения ( 1) и ( 2) ] протекает с выделением тепла. [1]
 |
Микроструктура покрытия сплавом реиий - хром иа меди ( х 10 000. [2] |
Восстановление водорода, например, в сульфаматном электролите происходит при ф 1 48 В. Однако выделение рения на катоде практически начинается при Ф 1 49 В. [3]
Рассмотри восстановление водорода на катоде, который химически не взаимодействует с водородом и не растворяет его. В этих условиях реакция восстановления не будет осложнена побочными явлениями и может быть изучена в чистом виде. Подходящим материалом для катода, удовлетворяющим поставленным требованиям, может служить ртуть. Кроме химической инертности относительно водорода, ртуть имеет еще одно существенное преимущество: величина жидкой поверхности катода может быть точно измерена и не будет подвергаться изменениям во время опыта. [4]
Рассмотрим восстановление водорода на катоде, который химически не взаимодействует с водородом и не растворяет его. В этих условиях реакция восстановления не будет осложнена побочными явлениями и может быть изучена в чистом виде. Подходящим материалом для катода, удовлетворяющим поставленным требованиям, может служить ртуть. Кроме химической инертности относительно водорода, ртуть имеет еще одно существенное преимущество: величина жидкой поверхности катода может быть точно измерена и не будет подвергаться изменениям во время опыта. [5]
Кинетика восстановления водорода доводит рассмотрение вопроса до образования из ионов Н молекул EU. Последние должны покидать поверхность электрода, без чего не может установиться стационарное состояние. [6]
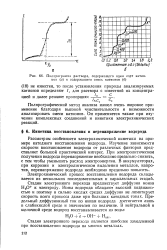 |
Подпрограмма раствора, содержащего один сорт катионов ( а и содержащего смесь катионов ( б. [7] |
Электрохимический процесс восстановления водорода складывается из нескольких последовательных и параллельных стадий. [8]
Катализ реакции восстановления водорода платиновой чернью увеличивается с увеличением рН раствора. Восстановительные свойства электрода, частично опущенного в раствор, а частично находящегося в атмосфере водорода, больше, чем электрода, полностью погруженного в раствор. [9]
В этих условиях восстановление водорода является единственным катодным процессом, поэтому катодный потенциал не может быть настолько большим, чтобы стало возможно пассивирование железа. [10]
В этих условиях восстановление водорода является единственным катодным процессом, поэтому катодный потенциал не может быть настолько большим, чтобы стало возможно пассивирование железа. [11]
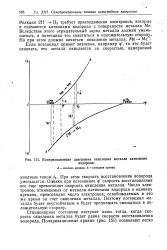 |
Поляризационная диаграмма окисления металла катионами. [12] |
При этом скорость восстановления водорода уменьшится. Однако при потенциале р скорость восстановления все еще превосходит скорость окисления металла. Число электронов, отнимаемых от металла катионами водорода в единицу времени, превосходит число электронов, освобождаемых в это же время за счет окисления металла. [13]
При этом скорость восстановления водорода уменьшится. [14]
Я представляет кинетику восстановления водорода на никеле в том же растворе. Верхняя кривая несколько причудливой формы выражает изменение потенциала в зависимости от lg i при анодной поляризации никеля. Экстраполяция прямой Н до пересечения с анодной кривой ( точка А) дает логарифм плотности тока, отвечающего стационарному потенциалу окисления никеля ионами водорода в данном растворе. Этот потенциал принят за начало координат. [15]
Страницы: 1 2 3 4