Катодное восстановление - анион
Cтраница 1
Катодное восстановление анионов сопровождается иногда специфическими для этого процесса затруднениями - спадами тока. На рис. 115 приведена i - ф-кривая для медного электрода в разбавленном пирофосфатном комплексном растворе. Такой эффект может быть объяснен переходом г - р-кривой через точку нулевого заряда и вызывается появлением сил отталкивания, которые возникают между отрицательно заряженной поверхностью металла ( катода) и анионами. Подобное влияние отрицательного заряда поверхности на анионы может проявиться различным образом. [1]
Катодное восстановление анионов сопровождается иногда специфическими для этого процесса затруднениями - спадами тока. На рис. 115 приведена i - ср-кривая для медного электрода в разбавленном пирофосфатном комплексном растворе. Такой эффект может быть объяснен переходом i - ф-кривой через точку нулевого заряда и вызывается появлением сил отталкивания, которые возникают между отрицательно заряженной поверхностью металла ( катода) и анионами. Подобное влияние отрицательного заряда поверхности я а анионы может проявиться различным образом. [2]
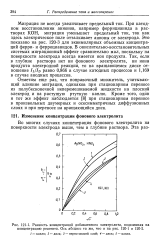
Катодное восстановление анионов сопровождается специфическими для этого процесса затруднениями - спадами тока. На рис. 96 приведена i-ф-кривая для электрода в разбавленном пирофосфатном медном комплексном растворе. Как видно из рисунка, при потенциале несколько более отрицательном, чем 0 05 в, ток резко уменьшается и процесс восстановления анионов СиР2О - тормозится. Такой эффект может быть объяснен пересечением i-ф-кривой потенциала нулевого заряда и вызывается появлением сил отталкивания, которые возникают между отрицательно заряженной поверхностью металла и анионами. [3]
Так, было показано, что скорость катодного восстановления анионов на отрицательно заряженной поверхности ртути в присутствии неорганических катионов, сдвигающих фрпотенциал в положительную сторону, возрастает в соответствии с уравнением (XII.28), причем увеличение скорости тем больше, чем выше заряд неорганического аниона. Восстановление анионов ускоряется и при увеличении радиуса катионов в ряду: Li Na К Rb Cs, так как с ростом радиуса катионов увеличивается их адсорбируемость на поверхности ртути. [4]
 |
Кругооборот соединений азота в ступени электролитической схемы с рекуперацией газов. [5] |
Концентрация ионов N01 и NOJ в электролите очень невелика даже при питании электролизера рекуператором, в котором присутствует заметное количество этих анионов, что свидетельствует о большой скорости катодного восстановления анионов азотной и азотистой кислот. [6]
 |
Разность концентраций добавленного электролита, поделенная на концентрацию реагента. Ось абсцисс та же, что и на 120 - 1 и 120 - 2. [7] |
Миграция не всегда увеличивает предельный ток. При катодном восстановлении анионов, например феррицианида в растворах КОН, миграция уменьшает предельный ток, так как здесь электрическое поле отталкивает анионы от электрода. Это показано на рис. 120 - 3 для эквимолярных объемных концентраций ферри - и ферроцианидов. В окислительно-восстановительных системах миграционный эффект сравнительно мал, поскольку на поверхности электрода всегда имеется ион продукта. Так, если в глубине раствора нет ни фонового электролита, ни иона продукта электродной реакции, то на вращающемся диске отношение IL / ID равно 0 866 в случае катодных процессов и 1 169 в случае анодных процессов. [8]
Си - - - - Си24 2е) или катодного восстановления анионов 52О - до 5О4 - к электрокаталитическим не относятся. [9]
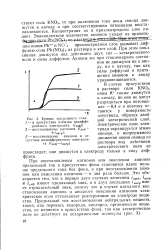 |
Кривые предельного тока. [10] |
При восстановлении катионов или окислении анионов предельный ток в присутствии фона становится вдвое меньше предельного тока без фона, а при восстановлении анионов или окислении катионов - в два раза больше. Это объясняется тем, что в первых двух случаях величины / пред, мигр и гдиф имеют одинаковый знак, а в двух последних jMlirp имеет отрицательный знак, потому что в случае катодного восстановления анионов и анодного окисления катионов электрическое поле отталкивает реагирующие на электроде вещества. [11]
Надо отметить, что теория влияния строения двойного слоя на перенапряжение, развитая А. Н. Фрумкиным на примере выделения водорода, применима также и к другим электрохимическим процессам. Так, согласно этой теории, скорость катодного восстановления анионов должна тормозиться при уменьшении ф1 - потенциала. Действительно, как сказано в примечании к стр. [12]
Страницы: 1