Металлотермическое восстановление
Cтраница 2
Метод металлотермического восстановления ВеС12 пока не используется промышленностью, но некоторые его варианты могут оказаться весьма перспективными, особенно при организации крупномасштабного непрерывного процесса. Разработка процесса связана с преодолением трудностей конструктивного характера. Но они, безусловно, преодолимы, тем более, что аналогичный процесс для титана уже предложен. Фторид бериллия ( tKlm 1327 С) позволяет вести процесс с получением расплавленного бериллия, образующего корольки металла. Из восстановителей наиболее подходит магний, так как щелочные металлы, например Na, обладают низкой температурой кипения. Кроме того, NaF - растворимое соединение, что затрудняет извлечение остатков BeF2 из шлака. Выше уже говорилось, что кальций дает с бериллием соединение СаВе13 и, кроме того, он дороже и грязнее магния. [16]
Реакции металлотермического восстановления, как правило, экзотермичны. [17]
Метод металлотермического восстановления не дает возможности получать чистые соединения, так как продукт реакции состоит из трех твердых фаз, разделение которых как физическими, так и химическими методами сопряжено с большими трудностями и поэтому он не имеет практического применения. [18]
Получается металлотермическим восстановлением HfOz, HfO4 или KaHfFe, образующихся после химической обработки циркониевых руд, содержащих гафний. [19]
При металлотермическом восстановлении окислов вольфрама W03, W40n, W02 алюминием, цинком, кальцием или магнием получают загрязненный порошок металлического вольфрама. Реакции, лежащие в основе этих восстановительных процессов. Избыток цинка и магния удаляется перегонкой или промыванием разб. Окислы вольфрама, не восстановленные до металлического вольфрама. [20]
Простота осуществления металлотермического восстановления наряду с возможностью использования полупродуктов металлургической переработки руд и концентратов привлекают к этому способу внимание исследователей. [21]
В результате металлотермического восстановления не удается получить титан высокой чистоты, требуемый для ряда областей применения. Для получения титана повышенной чистоты проводят рафинирование титана. Наиболее распространенным способом рафинирования является метод термической диссоциации галоидных соединений титана. Обычно применяют иодидный способ рафинирования. В этом случае черновой металл, подлежащий очистке, в результате взаимодействия с иодом образует иодиды. [22]
Необходимость применения металлотермического восстановления галогенидов при получении Ti, Zr, Hf обусловлена очень большой прочностью их оксидов, нитридов, карбидов. [23]
Необходимость применения металлотермического восстановления галогенидоа при получении Tl, Zr, Hf обусловлена очень большой прочностью их оксидов, нитридов, карбидов. [24]
Способна к металлотермическому восстановлению ( с алюминием или кальцием) до металлического титана. [25]
Для осуществления реакции металлотермического восстановления порошкообразную смесь окисла металла с металлом-восстановителем нагревают до расплавления одного из компонентов. В тех случаях, когда компоненты исходной смеси могут быть расплавлены за счет тепла, выделяющегося при протекании реакции восстановления, пользуются для инициирования реакции специальными зажигательными смесями. [26]
Поэтому в условиях металлотермического восстановления окислов ( при температурах 1200 - 1300 С) шлак получается в твердом, а уран - в капельножидком виде. [27]
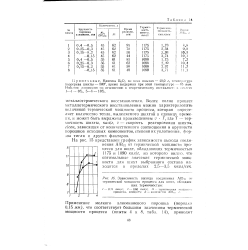 |
Зависимость выхода соединения А1В 2 от термической мощности процесса для шихт, обладающих термичностью. [28] |
Более полно процесс металлотермического восстановления можно характеризовать величиной термической мощности процесса, которая определяет количество тепла, выделяемого шихтой в единицу времени, и может быть выражена произведением v Т, где Т - тер-мичность шихты, кал / г, v - скорость реагирования шихты, г / сек, зависящая от количественного соотношения и крупности порошков исходных компонентов, степени их уплотнения, формы тигля и других факторов. [29]
Окись лития для металлотермического восстановления получают прокаливанием гидроокиси или карбоната лития при 800 С. [30]
Страницы: 1 2 3 4