Прямое электрохимическое восстановление
Cтраница 1
Прямое электрохимическое восстановление отдельных бензольных колец, по-видимому, не происходит, но его можно осуществить косвенным путем, проводя электролиз в присутствии различных восстанавливающих агентов, например солей щелочных металлов. [1]
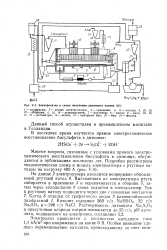 |
Электролизер и схема получения дитионита натрия. [2] |
Многие вопросы, связанные с условиями прямого электрохимического восстановления бисульфита в дитионит, обсуждаются в публикациях последних лет. [3]
Механизм процесса точно не установлен и может заключаться как в прямом электрохимическом восстановлении GeO до GeH4, так и в восстановлении германия выделяющимся атомарным водородом. [4]
Механизм процесса точно не установлен и может заключаться как в прямом электрохимическом восстановлении GeO § до GeH4, так и в восстановлении германия выделяющимся атомарным водородом. [5]
Амальгамный метод восстановления, являясь по существу разновидностью электрохимического, обладает целым рядом характерных положительных особенностей и в то же время исключает многие из трудностей прямого электрохимического восстановления органических соединений. В частности, амальгамами щелочных металлов можно восстанавливать органические соединения тех же классов, что и на электродах с высоким перенапряжением водорода; при амальгамном способе, так же как и при электрохимическом, можно осуществлять реакции гидродимеризации, которые каталитическим восстановлением обычно проводить не удается. [6]
Большое число примеров полярографических токов, имеющих каталитическую природу, приведены в книге С. Г. Майра-новского [10], а также в многочисленных работах Я. И. Турьяна и его сотрудников, С. И. Жданова, П. М. Зайцева и др. В частности, П. М. Зайцевым разработано интересное направление в аналитической химии - полярография каталитических систем с комплексообразователями, в которых проходит прямое электрохимическое восстановление окисленной формы иона металла - катализатора в двойном или смешанно-лигандном. [7]
Описана [7] возможная ситуация при восстановлении органических соединений в ГМФА. При низких плотностях тока идет прямое электрохимическое восстановление вещества. При повышении плотности тока вследствие кинетических или диффузионных ограничений скорость процесса замедляется, что приводит к возрастанию потенциала катода до потенциалов генерации электронов. Дальнейший процесс идет по двум механизмам - электрохимическому и химическому по реакции с сольватированными электронами. При высоких плотностях тока процесс в основном может идти по второму пути. Другой вариант - прямое восстановление органического соединения на катоде - не может идти вследствие невозможности переноса электрона к веществу из-за энергетических затруднений. В этом случае процесс протекает при высоких катодных потенциалах через химическое взаимодействие с сольватированными электронами. [8]
Существенным качественным отличием процесса ионизации кислорода на достаточно активных электродах из металлов-катализаторов ( Pt, Pd, Rh, Ir, Ru, Ag) и никеля является наличие только одной площадки предельного тока диффузии на поляризационной кривой электровосста новления кислорода. Это явление, с одной стороны, обусловлено меньшим перенапряжением процесса восстановления перекиси водорода, а с другой - возможностью прямого электрохимического восстановления кислорода в воду. Последняя реакция может протекать при диссоциативной хемосорбции кислорода. В отличие от ртутного и пирографитового электродов заполнение поверхности хемосорбированным кислородом на металлах-катализаторах вблизи стационарного потенциала достигает величин, близких к монослою, а на серебряном и никелевом электродах имеет место образование фазовых окислов. Это указывает на их высокое сродство к кислороду, что обеспечивает возможность протекания диссоциативной хемосорбции со значительной скоростью. [9]
Существенным качественным отличием процесса ионизации кислорода на достаточно активных электродах из металлов-катализаторов ( Pi, Pd, Rh, Ir, Ru, Ag) и никеля является наличие только одной площадки предельного тока диффузии на поляризационной кривой электровосста новления кислорода. Это явление, с одной стороны, обусловлено меньшим перенапряжением процесса восстановления перекиси водорода, а с другой - возможностью прямого электрохимического восстановления кислорода в воду. Последняя реакция может протекать при диссоциативной хемосорбции кислорода. В отличие от ртутного и пирографитового электродов заполнение поверхности хемосорбированным кислородом на металлах-катализаторах вблизи стационарного потенциала достигает величин, близких к монослою, а на серебряном и никелевом электродах имеет место образование фазовых окислов. Это указывает на их высокое сродство к кислороду, что обеспечивает возможность протекания диссоциативной хемосорбции со значительной скоростью. [10]
Страницы: 1