Дисульфид - титан
Cтраница 1
Дисульфид титана TiS2 получают 36, пропуская смесь пз сероводорода и тетрахлорида титана TiQ4 через раскаленную фарфоровую или кварцевую трубку ( работу вести под тягой. [1]
Дисульфид титана оседает в виде темного налета па стспке трубки. Оп содержит небольшое количество хлора. [2]
Дисульфид титана оседает в виде темного налета на стенке трубки. Он содержит небольшое количество хлора. [3]
Дисульфид титана в виде чешуек, по цвету и блеску похожих на латунь, получается пропусканием паров TiQ4 и H2S через накаленную фарфоровую трубку. При обычной температуре он устойчив. [4]
Дисульфид титана не растворим в воде и разведенных кислотах. [5]
 |
Прибор для получения TiS. 2 по реакции.| Плоскость ( 110 структуры сульфидов титана. [6] |
Дисульфид титана TiS2 может быть получен при взаимодействии рутила ТЮ2 с парами сероуглерода. [7]
Дисульфид титана является полупроводником п-типа [ 239, с. Электропроводность его при комнатной температуре составляет 1 4 - 103 ом 1 -см - 1; при комнатной температуре TiS2 и ZrS2 - типичные вырожденные полупроводники [ 239, с. Высокую электропроводность TiS2 и ZrS2 иногда объясняют отклонением от стехиометрии с образованием избытка металлических атомов. [8]
Дисульфид титана служит в органическом синтезе для производства амида и эфира ортотитановой кислоты. Некоторые сульфиды применяют для создания стойких коллоидных растворов серы. [9]
Дисульфид титана образует желтые кристаллы с металлическим блеском; при обычных условиях они устойчивы на воздухе, в воде и разбавленных кислотах ( H2S04, HC1 и др.)) взаимодействуют с расплавленным едким кали или с двуокисью углерода при нагревании; под действием HN03 или конц. [10]
Образуясь при сульфидировании в тончайших поверхностных пленках окислов, дисульфид титана не обладает достаточной адгезией, и вследствие различия постоянных решеток окислов и основного металла диспергируется и удаляется с поверхности при достижении соответствующих деформаций и температур при трении. Вследствие этого увеличение противозадир-ных свойств при сульфидировании для титана невелико. [11]
 |
Схема установки для синтеза халькогенидов. [12] |
Низшие сульфиды титана могут быть получены синтезом из элементов или восстановлением дисульфида титана водородом. При ампульном синтезе низших сульфидов после взаимодействия серы с титаном необходимо гомогенизировать препараты при более высоких температурах. [13]
Очень тугоплавкие сульфиды типа Э52 могут быть получены взаимодействием элементов при нагревании. Дисульфид титана представляет собой желтые кристаллы, ZrS2 - темно-коричневый порошок. [14]
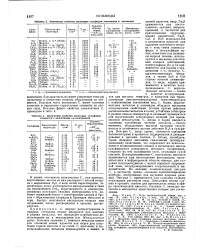 |
Физические свойства некоторых сульфидов лаитанидов и актинидов.| Физические свойства некоторых сульфидов элементов с валентными яр-электронами. [15] |
Страницы: 1 2