Тяжелый азот
Cтраница 1
Тяжелый азот и дейтерий помогли также установить, что и азотсодержащие соединения в организме непрерывно и очень быстро обновляются. [1]
Образовавшийся тяжелый азот содержит излишек нейтронов: 9 нейтронов на 7 протонов. [2]
При введении тяжелого азота крысам в виде N15H меченый азот переходит в креатин, причем переносчиками его служат аминокислоты. [3]
С помощью тяжелого азота были получены некоторые данные о путях синтеза нуклеиновых кислот. [4]
При введении тяжелого азота крысам в виде N16H меченый азот переходит в креатин, причем переносчиками его служат аминокислоты. [5]
При помощи тяжелого азота и радиоактивного фосфора были достигнуты значительные успехи в изучении метаболизма пуриновых соединений, нуклеиновых кислот и нуклеопротеинов. [6]
Благодаря использованию тяжелого азота установлены исключительно важные факты, меняющие сложившиеся представления об азотном питании растений. Прежде считали, что образование органических азотистых веществ идет почти исключительно в надземных частях растения за счет минеральных соединений азота, поступивших через корни. В действительности аммиачный азот в корнях уже через 10 - 15 минут после поглощения его из внешнего раствора превращается в аминокислоты, которые передвигаются в надземную часть. Теперь нельзя уже считать корни только органами поглощения, ибо именно в них образуется не менее 14 аминокислот из общего числа около 20, необходимых для синтеза молекулы белка. [7]
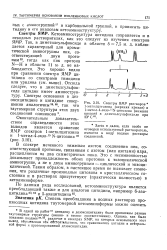 |
Спектры ЯМР растворов 1-метилцитозина ( верхняя кривая и 1-метил - 4-экзо - 15Ы - цитозина ( нижняя кривая в диметилсульфоксиде при 23 С 62. [8] |
В спектре меченного тяжелым азотом соединения пик, соответствующий протонам, связанным с азотом ( или азотами) ядра, расщепляется на два симметричных пика. Это с несомненностью доказывает принадлежность обоих протонов к экзоциклической аминогруппе, а не к двум иминогруппам - циклической и экзоциклической. Таким образом, в настоящее время не вызывает сомнения, что различные производные цитозина в кристаллическом состоянии и в растворах присутствуют ( практически полностью) в кетоаминоформе. [9]
С помощью дейтерия и тяжелого азота Шенгеймером были выяснены пути образования и превращений креатина в организме. Путем введения в пищу животного разных аминокислот, меченных дейтерием в N15, было установлено, что для образования креатина мышц нужны три из них. Глицин дает креатин с N15 в аминогруппе ( но не в амидиновой); аргинин доставляет амидиновую группу с N15 в ней, а метионин вводит метильную группу, меченную дейтерием. [10]
Работы с аммиаком, меченым тяжелым азотом N15, показали, что аммиак может быть использован для синтеза аминокислот и что альфа-аминогруппа каждой аминокислоты не представляет только структурную статическую часть ее молекулы: она все время находится в состоянии динамического обмена с другими аминогруппами. Выяснилось также, что обратимые системы, участвующие в процессах обмена, нельзя рассматривать, как действующие таким образом, что соответствующий процесс идет сначала в одном направлении, а потом в другом. В таких системах обе реакции ( прямая и обратная) протекают в обоих направлениях одновременно. Поэтому весь процесс в целом приобретает крайнюю динамичность. [11]
Кормление разными аминокислотами, меченными тяжелым азотом, показало, что они неодинаково ведут себя в организме. Тирозин дает больше всего N15 в белках печени и меньше - в белках плазмы. Обратное соотношение наблюдалось для лейцина, причем в белках печени за семь дней половина его заменялась меченым. Особенно подробно изучалась судьба глицина в теле. В печени введенный меченый глицин быстро обменивается с ранее содержавшемся в ней глицином других тканей. В печени крыс такое обновление глицина достигает 10 % в день. [12]
Кормление разными аминокислотами, меченными тяжелым азотом, показало, что они неодинаково ведут себя в организме. Тирозин дает больше всего N16 в белках печени и меньше - в белках плазмы. Обратное соотношение наблюдалось для лейцина, причем в белках печени за семь дней половина его заменялась меченым. Особенно подробно изучалась судьба глицина в теле. В печени введенный меченый глицин быстро обменивается с ранее содержавшемся в ней глицином других тканей. В печени крыс такое обновление глицина достигает 10 % в день. [13]
Исследование механизма реакций азотсодержащих соединений с помощью тяжелого азота 18N было начато А. И. Бродским и Б. А. Геллером, а затем широко продолжено Б. А. Геллером с сотрудниками. Был выяснен источник азота во вторичных аминах при их образовании из двух молекул первичных аминов, в замещенных феназинах при их получении из нитрозонафтиламинов и арила-минов, в тетрагидрокарбазоле при его образовании из фенилгидра-зона циклогексанона. [14]
Это число было найдено из скорости накопления тяжелого азота в крови. Оно, повидимому, не очень достоверно. [15]
Страницы: 1 2 3 4