Беспорядочное вращение
Cтраница 1
Беспорядочное вращение звеньев в пространстве приводит к запутыванию молекулы в клубок. Ясно, что в таком состоянии ее энтропия больше, чем если она вытянута, потому что число свернутых расположений гораздо больше, чем растянутых. [1]
В интервале от 125 до температуры плавления ион [ N0s ] - принимает шаровую форму вследствие беспорядочного вращения около одной точки, а не около оси, как в предыдущем случае. [2]
 |
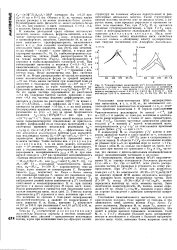
Полиморфизм парафина С2вНво. [3] |
В интервале от 125 С до температуры плавления ( 169 6 С) ион NOs принимает шаровую форму вследствие беспорядочного вращения около одной точки, а не около оси, как в предыдущем случае. [4]
Физически это означает, что немати-ческая упаковка улучшает условия для вращения молекул вокруг продольных осей по сравнению с их беспорядочным вращением в изотропной фазе. На рис. 2.15 воспроизведен ход параметров gj и gj в зависимости от вы-соты потенциального барьера, определяющего нематиче-ский порядок. [5]
Точнее говоря, энергия взаимодействия звеньев слабо зависит от этого поворота в пространстве, так что при комнатных температурах осуществляется как бы свободное, беспорядочное вращение, напоминающее движение несвязанных молекул газов. [6]
 |
Относительное положение вращающейся колонны и скважины 12. [7] |
В процессе бурения могут наблюдаться беспорядочные вращения, сопровождающиеся биениями, что характерно для режимов, близких к резонансным или к условиям, при которых теряется устойчивость прямолинейной формы. [8]
Поскольку в ковалентном остове полипептидной цепи все связи одинарные, можно было бы ожидать, что полипеп-тйд способен принимать в пространстве бесконечное число конформации. Более того, естественно было бы предположить, что конформация полипептида претерпевает постоянные изменения вследствие теплового движения и беспорядочного вращения участков цепи вокруг каждой из одинарных связей кова-лентного остова. Поэтому может показаться парадоксальным тот факт, что полипептидная цепь нативного белка в нормальных биологических условиях-при обычной температуре и нейтральных значениях рН - имеет только одну или очень небольшое число конформации. Эта нативная конформация достаточно устойчива: если выделение белка вести осторожно, избегая воздействий, приводящих к развертыванию цепей и денатурации, то выделенный белок может полностью сохранить свою биологическую активность. Это свидетельствует о том, что вокруг одинарных связей полипептидного остова в нативных белках свободное вращение невозможно. [10]
Столь малые частички при комнатной темп-ре движутся с тепловыми скоростями ir - 10 см - с 1 и характерное время, за к-рое частичка изменяет направление движения, составляет f - p1V0 / 3mvi0 - 10 - 10 с. За это время частица перемещается на расстояние - 0 1 им. Беспорядочное вращение частиц таково, что они поворачиваются на угол - 1 рад за время броуновского вращения TB-Ji ( d0 26) sri / 2A7 - l мкс при ris я10 - гг-см-1 - с-1. [12]
Тепловое движение макромолекул в растворе имеет множественную природу. Во-первых, так же как у малых молекул, имеет место поступательное броуновское движение, создающее осмотическое давление. Во-вторых, происходит вращательное броуновское движение макромолекул в целом. В-третьих, существует колебание всех звеньев макромолекулы относительно друг друга. В-четвертых, внутри каждой полимерной цепи происходит внутримолекулярное броуновское движение, складывающееся из вращений всех звеньев цепи друг относительно друга. В результате таких беспорядочных вращений цепь непрерывно деформируется, образуя хаотический свернутый клубок, центр тяжести которого также перемещается. Макромолекула движется как свернутая в клубок змея, находящаяся в непрерывном и притом беспорядочном движении. Наличие в макромолекуле огромного количества внутренних степеней свободы и связанной с ними огромной внутримолекулярной энтропии является причиной многих своеобразных качественных отличий растворов полимеров от обычных растворов. [13]
Страницы: 1