Время - термостабильность
Cтраница 1
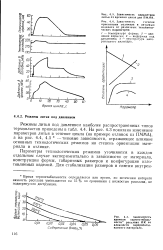 |
Зависимость степени. [1] |
Время термостабильности определяется как время, по истечении которого вязкость расплава уменьшается на 15 % по сравнению с вязкостью расплава, не подвергнутого деструкции. [2]
Время термостабильности т ( в мин) - продолжительность индукционного периода до начала выделения НС1 в свободном виде из ПВХ или его смесей со стабилизаторами и другими добавками при выбранной температуре. [3]
Время термостабильности - индукционный период до момента выделения НС1 в свободном состоянии из композиций ПВХ металлсодержащий стабилизатор-акцептор НС1 при фиксированной ( часто 175 С) температуре деструкции полимера. [4]
Например, время термостабильности характеризует максимально допустимое время переработки ПВХ конкретным методом и одновременно долговечность материалов и изделий из этого полимера. [5]
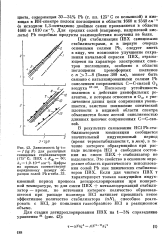 |
Зависимость lg т / ( lg N для различных свинцовых стабилизаторов ( 175 С. ПВХ с Кф 60. k 1 9 - 10 - сек-1. Цифры на прямых соответствуют порядковому номеру образцов солей РЬ в 33. [6] |
В результате связывания НС1 РЬ-ста-билизаторами композиции сообщается значительный индукционный период ( время термостабильности т, в мин), в течение которого образующийся при распаде полимера НС1 в свободном состоянии из смеси ПВХ стабилизатор не выделяется. Это свойство в основном определяет область практического использования солей РЬ как химических стабилизаторов ПВХ. [7]
ПВХ, в том числе и в инертной атмосфере, и заметно увеличивающие время термостабильности т композиции. Эта группа ООС сочетает функции металлсодержащих химических стабилизаторов ПВХ - акцепторов НС1 с функцией ингибиторов химических процессов и поэтому весьма эффективна при стабилизации ПВХ. [8]
В качестве критерия оценки стойкости к тепловому старению были выбраны относительное удлинение при разрыве и время термостабильности. [10]
При использовании смесей металлических мыл или других солей металлов часто наблюдается суммарный эффект по показателю времени термостабильности ПВХ-композиций, определяемый эффективностью стабилизаторов-акцепторов НС1 и скоростью элиминирования НС1 из ПВХ. Однако при совместном присутствии карбокси-латов металлов Са, Ва, Pb, Cd, Zn и Mg HC1 имеет тенденцию реагировать сначала с солями металлов Па группы ( Са, Ва, Mg), образуя менее вредные для процесса дегидрохлорирования ПВХ хлориды металлов. [11]
Амиды кислот фосфора, понижая скорость реакции дегидрохлорирования и подавляя действие поливалентных металлов, в то же время увеличивают время термостабильности. [12]
Проведенные ранее исследования влияния пирокатехинфос-фитов на поливинилхлорид ( ПВХ) показали, что они снижают скорость дегидрохлорирования полимера, подавляют вредное действие поливалентных металлов, но не увеличивают времени термостабильности, являющегося одним из важных показателей для нормальной переработки ПВХ. [13]
После термической экспозиции в течение 1 ч при 175 С наблюдается уменьшение квадрупольного расщепления до 2 9 мм / сек. При нагревании композиции свыше времени термостабильности т ( 3 ч) квадру-польное расщепление увеличивалось до 3 0 8 мм / сек и соответствовало ( C4H9) 3SnCl, что и подтверждают ГР-спектры гидролизованных образцов. Аналогичные результаты получены для дикаприлата дибутилолова. [14]
В силу рецептурных факторов эмульсионный ПВХ обычно содержит соду или щелочь, двузамещенный фосфорнокислый натрий и другие примеси. Их присутствие способствует частичному связыванию выделяющегося из полимера НС1, что приводит к кажущемуся повышению стабильности макромолекул ПВХ ( увеличение времени термостабильности и температуры разложения ПВХ), но не предотвращает главного - возможности деструкции полимерных цепей. Более того, увеличивается содержание примесей, что обычно отрицательным образом сказывается при переработке ПВХ и эксплуатации материалов или изделий на его основе. [15]
Страницы: 1 2
