Одноэлектронный интеграл
Cтраница 2
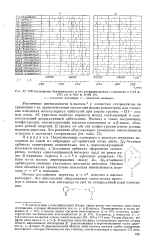 |
УФ-поглощение бензимидазола и его мотилзамещенных гомологов в 0 01 н. [16] |
Несвязывающие электроны в молекуле пиридина находятся на одной из гибридных s / r - орбиталей атома азота. Атомная орбиталь симметрична относительно оси z, перпендикулярной плоскости кольца, а 2я - атомная орбиталь сферически симметрична, поэтому одноэлектронный интеграл szpzd не равен нулю. Однако из-за малого перекрывания между 2л -, 2 / 2-атомными орбиталями значение указанного интеграла невелико. Именно этим объясняется сравнительно невысокая интенсивность перехода п - л в пиридине. [17]
Отталкивание между остовами представляет собой более трудную проблему. Простейшим решением было бы принять его равным полному межэлектронному отталкиванию, как это делалось в расчетах п-электронных систем, однако в данном случае такое допущение приводит к предсказанию слишком коротких длин связей. Причину этого можно легко объяснить. Если мы принимаем уравнение (10.37) для притяжения электронов к остовам и аналогичное выражение для отталкивания между остовами, то результирующий классический ку-лоновский потенциал между двумя нейтральными атомами в молекуле обращается в нуль при всех межъядерных расстояниях, поскольку отталкивание между электронами и отталкивание между остовами точно компенсируют притяжение электронов к остовам. В действительности межэлектронное отталкивание меньше величины, вычисленной в классическом приближении, вследствие обменной поправки к отталкиванию между парами электронов с параллельными спинами, тогда как притяжение электронов к остовам больше вычисленного по классическим формулам вследствие квантовомеха-нических эффектов, проявляющихся в одноэлектронных интегралах ( см. разд. В расчетах л-электронных систем эта трудность не возникает, так как в этих случаях предполагается наличие жесткого остова из локализованных связей, определяющего геометрию молекулы. При учете ст-электронов нет причин, препятствующих слиянию атомов. [18]
Страницы: 1 2