Резонансный интеграл - связь
Cтраница 1
Резонансный интеграл связи азот-азот в диазониевой группировке растет с увеличением перекрывания р-орбиталей атомов азота и, следовательно, с уменьшением расстояния между ними. [1]
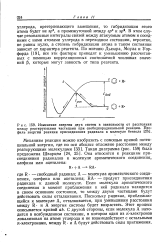 |
Изменение энергии двух систем в зависимости от расстояния между реагирующими частицами при свободнорадикальной реакции. Профиль энергии реакции присоединения радикала к молекуле бензола. [2] |
В этом случае резонансные интегралы связей между атакуемым атомом и соседними с ними атомами углерода в переходном состоянии, вероятно, не равны нулю, а степень гибридизации атома в таком состоянии зависит от характера реагента. По мнению Дьюара, Моула и Уор-форда [19], все эти факторы приводят к уменьшению рассчитанных с помощью корреляционных соотношений числовых значений Р, которые могут зависеть от типа реагента. [3]
К сожалению, существуют разные мнения относительно величины резонансного интеграла связи С-О. На основании подробных расчетов молекулы формальдегида Браун и Коллер [20] принимали рсо - Р, но несколько позже Пилар и Моррис [91] предложили значительно меньшее значение рсо / юР - Величина куло-новского интеграла атома кислорода ( ссо) также не совсем точна, хотя Браун и Коллер предполагали, что она должна быть близка к соответствующей величине для-атома азота в пирроле. [4]
При расчете таких сверхсопряженных систем по методу молекулярных орбит резонансные интегралы обычных кратных и постулированных псевдократных связей принимаются пропорциональными резонансному интегралу связи С С в этилене с длиною 1 33 А, причем коэффициенты пропорциональности рассматриваются как некоторая функция длин связей. Напрашивается предположение, что длина изолированной связи С-С с порядком, равным 1, должна быть не 1 54 А, как в этане, а больше: - 1 58 А. При помощи кривой порядок связи - длина связи Малликен находит, что длина связи С - Н в метильной группе метилацетилена Должна быть более длины нормальной связи С - Н приблизительно на 0 001 А. Однако это предсказание оказалось верным только качественно: связь С - Н в метилацетилене действительно удлинена, но это удлинение равно примерно 0 02 А ( см. сводку № 25 на стр. [5]
При расчете энергии переходного состояния рассматривается только одна орбиталь реагента: с парой электронов, если это нуклеофил, с одним электроном, если радикал, и без электронов, если это электрофил. Задается резонансный интеграл связи PC-NU, образующейся между реагентом и субстратом. [6]
В ароматических полисульфидах положение энергетических уровней молекулы и в основном, и в возбужденном состоянии должно определяться 2п оптическими электронами атомов серы и т: - электронами бензольных колец. При расчете значения резонансного интеграла связи С-S и ку-лоновского интеграла атома серы были взяты такими же, как и для дифенилсульфида. Резонансный интеграл связи S-S выбирался равным 0 8jl На рисунке представлена схема энергетических уровней ряда рассчитанных полисульфидов. Наиболее длинноволновая полоса поглощения обусловлена переходом электрона с последнего заполненного молекулярного уровня на возбужденный уровень бензольного кольца. Увеличение числа атомов серы в цепочке приводит к повышению последнего заполненного уровня и, следовательно, к смещению полосы поглощения в более длинноволновую область спектра. Число возможных электронных переходов с энергией 1 - т - 2 Р растет с числом п, что должно приводить к наложению полос поглощения. Поэтому в области 200 - 400 ммк отмечается почти сплошной спектр поглощения полисульфидов с очень слабо выраженными максимумами. [7]
В ароматических полисульфидах положение энергетических уровней молекулы и в основном, и в возбужденном состоянии должно определяться 2п оптическими электронами атомов серы и я-электронами бензольных колец. При расчете значения резонансного интеграла связи С-S и ку-лоновского интеграла атома серы были взяты такими же, как и для дифенил сульфида. На рисунке представлена схема энергетических уровней ряда рассчитанных полисульфидов. Наиболее длинноволновая полоса поглощения обусловлена, переходом электрона с последнего заполненного молекулярного уровня на возбужденный уровень бензольного кольца. Увеличение числа атомов серы в цепочке приводит к повышению последнего заполненного уровня и, следовательно к смещению полосы поглощения в более длинноволновую область спектра. Число возможных электронных переходов с энергией 1 - - 2 р растет с числом п, что должно приводить к наложению полос поглощения. Поэтому в области 200 - - - 400 ммк отмечается почти сплошной спектр поглощения полисульфидов с очень слабо выраженными максимумами. [8]
Расчеты по методу МО в приближении Хюккеля свидетельствуют о том, что все эти системы стабилизированы вследствие циклической делокализации я-электронов. Энергия циклической делокализации зависит от электроотрицательности гетероатома и резонансного интеграла связи С-X. При увеличении электроотрицательности гетероатома энергия уменьшается. [9]
Мы переходим к рассмотрению группы методов, позволяющих получать величины, которые можно считать приближениями к результатам метода МОХ. Будем искать решение для системы, которая мало отличается от исходной; пусть, например, новая система отличается значением кулоновского интеграла в положении ц либо значением резонансного интеграла связи ра. [10]
В ароматических полисульфидах положение энергетических уровней молекулы и в основном, и в возбужденном состоянии должно определяться 2п оптическими электронами атомов серы и т: - электронами бензольных колец. При расчете значения резонансного интеграла связи С-S и ку-лоновского интеграла атома серы были взяты такими же, как и для дифенилсульфида. Резонансный интеграл связи S-S выбирался равным 0 8jl На рисунке представлена схема энергетических уровней ряда рассчитанных полисульфидов. Наиболее длинноволновая полоса поглощения обусловлена переходом электрона с последнего заполненного молекулярного уровня на возбужденный уровень бензольного кольца. Увеличение числа атомов серы в цепочке приводит к повышению последнего заполненного уровня и, следовательно, к смещению полосы поглощения в более длинноволновую область спектра. Число возможных электронных переходов с энергией 1 - т - 2 Р растет с числом п, что должно приводить к наложению полос поглощения. Поэтому в области 200 - 400 ммк отмечается почти сплошной спектр поглощения полисульфидов с очень слабо выраженными максимумами. [11]
 |
Схема волновых функций стильбена. [12] |
Энергия молекулярной орбитали зависит от числа ее узловых плоскостей. Наиболее стабильная орбиталь имеет все коэффициенты при атомных орбиталях одного знака, наиболее нестабильная имеет узел ( меняет знак) на каждой связи ( см. стр. Если уменьшить величину резонансного интеграла связи между атомами г и s ( Prs), уровни орбиталей, имеющих узлы на данной связи, будут понижаться, а уровни орбиталей, не имеющих узлов, - повышаться. Уменьшение резонансного интеграла является мерой уменьшения взаимодействия между электронами частей молекулы, расположенных по разные стороны от этой связи. [13]
Тогда получающаяся система формально аналогична бензолу, так как в обоих случаях имеется 6 атомных л-орбит и 6 я-электронов. Это сходство еще сильнее увеличивается благодаря используемым, Лонге-Хиггинсом параметрам, так как они выбраны в предположении, что в тиофене на каждой атомной я-орбите действительно находится один электрон. Однако величина резонансного интеграла связи С-S принималась меньшей, чем р, так что молекула тиофена должна быть аналогична гипотетической молекуле бензола, в которой частично локализована одна двойная связь. [14]
Страницы: 1