Интенсивность - диффузия
Cтраница 1
Интенсивность диффузии очень сильно увеличивается с повышением температуры. При увеличении температуры, начиная от комнатной, на каждые 10 - 15 коэффициент диффузии возрастает примерно вдвое. Средние значения коэффициента самодиффузии металлов составляют 1 - 10 - 17 м2 / с при температуре на 200 - 500 ниже точки плавления. Приблизительно такие же значения характерны для элементов, атомы которых замещают атомы основного металла в узлах кристаллической решетки. Вблизи точки плавления коэффициент диффузии в этих случаях достигает величины порядка Ы ( Н2 м2 / с. Для элементов, атомы которых размещаются в междуузлиях решетки, характерны значительно большие коэффициенты диффузии - примерно в 103 - 104 раз. Названные выше величины для твердых металлов соответствуют диффузии внутри зерен. Диффузионное перемещение атомов по границам зерен происходит в 100 - 1000 раз интенсивнее. [1]
Интенсивность диффузии ионов железа в оксидной пленке сильно зависит от температуры. На рис. 4.6 показан характер изменения константы скорости окисления железа в водяном паре в координатах Аррениуса. В области температур 570 - 630 С происходит качественное изменение характера окисления, что объясняется изменением механизма окисления железа в соответствии с диаграммой равновесия железа в водяном паре. [2]
Влажность стимулирует интенсивность диффузии водно-солевых комплексов и является главным фактором, определяющим слеживаемость удобрений. Влагосодержа-ние продукта в процессе хранения изменяется в зависимости от его гигроскопичности. [3]
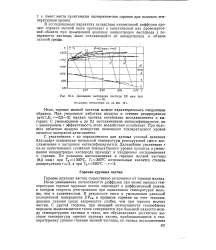 |
Динамика выгорания частицы 8 5 мкм при г10. [4] |
Из-за уменьшения интенсивности диффузии при менее высоких температурах горение крупных частиц переходит в диффузионный режим, в котором скорость реагирования при одинаковых температурах меньше, чем в кинетическом. В результате этого и уменьшения удельной реакционной поверхности / / Уем в процессе горения за счет тепловыделения газовая среда нагревается слабее, чем при горении мелких частиц. [5]
 |
Схема расположения - потенциальных ям в шлаке и металле. [6] |
При сравнении интенсивностей диффузии и перехода ионами О2 - и Fe2 границы шлак - металл нужно заметить следующее. Диффузия закиси железа является стадией, параллельной переходу границы раздела. Находящиеся здесь ионы О2 - и Fe2 либо переходят в металл, либо движутся от него в направлении к газовой фазе. Иначе говоря, указанные ионы участвуют одновременно в двух параллельных процессах. [7]
К - коэффициент, зависящий от интенсивности диффузии и, следовательно, от интенсивности контакта реагентов ( барботаж, перемешивание и т.п.); F - поверхность контакта реагентов; Р - парциальное давление олефина / ( с) - множитель, зависящий от концентрации серной кислоты. [8]
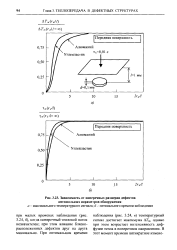 |
Зависимость от поперечных размеров дефектов оптимальных параметров обнаружения. [9] |
АТт, однако при этом возрастает интенсивность диффузии тепла в поперечном направлении. [10]
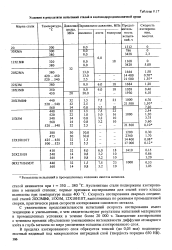 |
Условия и результаты испытаний сталей в азотоводородоаммиачной среде. [11] |
Замедление азотирования с течением времени обусловлено уменьшением интенсивности диффузии атомарного азота в глубь металла по мере увеличения толщины азотированного слоя. [12]
Пористая структура катализатора является важнейшим фактором, определяющим интенсивность диффузии реагентов внутри гранулы катализатора. VII будут изложены способы численной оценки эффективных коэффициентов диффузии с помощью моделей пористой структуры. [13]
Взаимодействие между диффундирующей средой и полимером приводит к увеличению интенсивности диффузии. [14]
Взаимодействие между диффундирующей средой и полимером приводит к увеличению интенсивности диффузии. [15]
Страницы: 1 2 3 4