Вторичный азот
Cтраница 1
Вторичный азот триптофана, пролина и оксипролина, вторичный и третичный азот гистидина, гуанидиновая группа аргинина и. Первичная аминогруппа большинства аминокислот количественно реагирует с азотистой кислотой. Глицинпептиды образуют 120 % от рассчитанного теоретически количества азота. Лизин реагирует с азотистой кислотой а - и е-аминогруппами, причем s - аминогруппа реагирует медленнее. [1]
При длительном нагревании анабазина с избытком йодистого метила происходит, очень гладко, метилирование вторичного азота, но одновременно с этим происходит и присоединение йодистого метила к третичному азоту, так что в результате получается иодистоводородная соль иодметилата метиланабазина. [2]
Во всех пиперидиновых продуктах окисления хинина и цинхонина азот вторичен, тогда как в хинине нет вторичного азота. [3]
&2 - Атомы серы эффективны как доноры потому, что являются сильными нуклеофильными агентами, гидроокись - потому, что она депротонирует вторичный азот, образуя основание, активное в реакциях с диссоциативным механизмом. Такое поведение, которое очень напоминает катализируемый основанием гидролиз при замещении в октаэдрическом комплексе, не наблюдается в отсутствие кислотных протонов. [4]
Но так как выход аминоанабазина был чрезвычайно низок, мы перешли к амидированию М - аштиланабазина [2], легко получаемого из анабазина, где отсутствие вторичного азота позволяло ожидать увеличения выхода. С, второй - в виде бесцветного, густого, некристаллизующегося масла, которое было охарактеризовано через пикрат. [5]
Тот факт, что N-метилмочевина ( 175, R1 Me, R2 Н) превращается в ( 177, R1 Me, R2H), согласуется с образованием О-ацильного интермедиата, хотя вторичный азот должен быть более нуклеофильным при прямой атаке на ацилирую-щий агент. [6]
Кажется также, что увеличение размера кольца в четырехдентатном лиганде ЫН2 ( СН2) ЖЫН ( СН2) ЙКН ( СН2) Н2 от у ( или х) 2 до 3 стабилизирует в его комплексах состава [ Со ( амин) С12 ] структуру XLIV по сравнению со структурой XLIII, возможно, вследствие того, что при шестичленном кольце возникают меньшие напряжения валентных углов у пирамидальных центров атомов вторичного азота. [7]
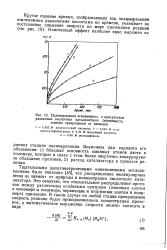 |
Полимеризация этиленимина в присутствии. [8] |
Тщательными дилатометрическими кинетическими исследованиями было показано [16], что распределение молекулярных весов не зависит от природы и концентрации кислотного катализатора. Это означает, что относительное распределение протонов между различными основными центрами ( аминным азотом в мономере и полимере, первичным и вторичным азотом в полимере) одинаково. [9]
Этот алкалоид, один из атомов азота которого является вторичным, позволяет получить целый ряд производных, образующихся путем введения радикалов вместо водорода, стоящего при этом вторичном азоте. [10]
В спектре ( рис. 5.14) наблюдаются два сигнала протонов метиленовых групп, каждый из которых расщеплен на пять пиков. Сигнал в слабом поле ( а - е) отвечает метилольным группам при третичном атоме азота N ( CH2OH) 2, а в сильном поле ( f - j) - при вторичном азоте NHCH2 ОН. Таким образом, по спектру ПМР в D20 идентифицированы 8 из 9 возможных ММА и определены константы скорости метилоларования. [11]
Однако, имея в виду, что в молекуле анабазина азот пиперидиново-го ядра более основной, чем азот пиридинового цикла, мы рассчитывали получить монохлоргидрат при недостаточном количестве хлористого водорода прежде всего за счет вторичного азота анабазина. [12]
Достигают разделения алкалоидов также получением их производных: Алкалоиды способны давать с теми или иными реактивами соединения, отличающиеся по свойствам от других алкалоидов, не вступающих в реакцию. Для этого требуется лишь, чтобы данный алкалоид при регенерации из производного существенно не изменялся. Примером может служить отделение алкалоидов с вторичным азотом от алкалоидов с третичным азотом. Первые при обработке азотистой кислотой ( NaNC2 H2SOi) дают нитрозосоединения R N-NO, а вторые при этом не изменяются. Полученное нитрозосоединение имеет более высокую температуру кипения и может быть отделено от третичного основания отгонкой под вакуумом. Так, алкалоиды растения Anabasis aphylla - анабазин и лупинин - имеют весьма близкие точки кипения, но после обработки нитрозирующей смесью нитрозоанабазин имеет температуру кипения на 50 - 60 выше, чем лупинин, благодаря чему его и возможно отделить от лупинина. Если подвергнуть бензоилированию смесь алкалоидов вторичного и третичного характера, вторичные дают бен-зоильное производное R N-СО-CeHs, имеющее характер кислотного амида и не растворимое в кислотах, благодаря чему оно отделяется от третичного амина. Гидролизом полученного бензоильного производного затем получают исходный алкалоид. В большинстве случаев приходится пользоваться различными способами, комбинируя их между собой сообразно с обстоятельствами. [13]
Растение это носит название Anabasis aphylla. О еем было известно только, что оно ядовито и что скот его не ест. Была установлена структура алкалоида, представляющая известную аналогию с никотином, с той лишь разницей, что в анабазине два шестичленных кольца, в отличие от пятичленного в никотине, и вторичный азот. Это строение было установлено на основе того, что при окислении анабазин дает никотиновую кислоту, а при дегидрировании - синтетически полученный а, 3-дипиридил. Этим была установлена структура анабазина, и мы перешли к изучению различных его производных. Близость строения анабазина к никотину, который давно применяется в качестве инсектицида, привела к мысли, что и анабазин может быть использован для этой цели. [14]
Страницы: 1