Интервал - потенциал
Cтраница 1
Интервал потенциалов второй задержки на кривой анодной поляризации в боратно-буферном растворе ( вторая стадия) почти совпадает с интервалом потенциалов на кривой анодной поляризации индия в 1 Н КОН, где происходит пассивация индиевого электрода вследствие образования I п2О3 Гальваностатические кривые еще не позволяют характеризовать природу и устойчивость продуктов, которые возникают на той пли иной стадии на поверхности анода. [1]
Интервал потенциалов, в котором наблюдается тормозящее действие добавок, определяется областью их адсорбции. Применение адсорбирующихся веществ ионного типа позволяет исследовать торможение при потенциалах, значительно удаленных от точки нулевого заряда. Так, при введении в раствор сульфосали-циловой кислоты ( поверхностно-активный анион) наблюдается торможение при потенциалах положительнее - 0 2 в ( нас. [2]
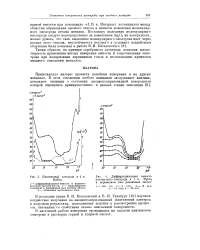 |
Платиновый электрод в 1 н. H2S04.| Дифференциальная емкость платинового электрода в н. HaSCU в переменном токе различных частот. [3] |
Интервал потенциалов между областью образования высшего окисла и началом выделения молекулярного кислорода весьма невелик. [4]
Интервал потенциалов, в котором наблюдается тормозящее действие добавок, определяется областью их адсорбции. Применение адсорбирующихся веществ ионного типа позволяет исследовать торможение при потенциалах, значительно удаленных от точки нулевого заряда. Так, при введении в раствор сульфосали-циловой кислоты ( поверхностно-активный анион) наблюдается торможение при потенциалах положительнее - 0 2 в ( нас. [5]
Интервал потенциалов поляризации также ограничивает возможности применения различных стационарных электродов. Например, ртутные стационарные электроды всех видов не работают в положительной области потенциалов поляризации. Выдавливаемые ртутные электроды обрываются при. [6]
Интервал потенциалов поляризации приводится нами в этих прописях лишь в тех случаях, когда в оригинальных публикациях отсутствуют сведения о потенциалах пиков. Кроме того, при применении концентрированных кислот указывается только их название. [7]
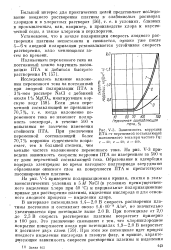 |
Зависимость коррозии ПТА от переменной составляющей наложенного тока при частоте Гц. [8] |
В интервале потенциалов 1 4 - 2 0 В скорость растворения платины постоянна и составляет около 1 6 - 10 - 4 А / м2, но значительно увеличивается при потенциале выше 2.0 В. При потенциале от 2 0 до 2 5 В скорость растворения платины возрастает примерно в 100 раз. [9]
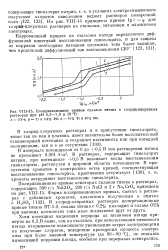 |
Поляризационные кривые сплавов титана в хлорид-хлоратных. [10] |
В интервале потенциалов от 0 до 0 5 В ток растворения титана не превышает 0 001 А / ма. В растворах, содержащих гипохлорит натрия, при потенциале 0 5 В возникает волна восстановления гипохлорита, растянутая в широкой области потенциалов. [11]
В интервале потенциалов от - f - 0 2 до - 0 2 в катионы тропилия не восстанавливаются. [12]
В интервале потенциалов от - 0 6 до - 1 9 в предельный ток восстановления РЬ2 остается постоянным. Если затем уменьшить концентрацию свинца, то полярограмма будет соответствовать кривой В, со значительно меньшим предельным током. [13]
В интервале потенциалов, в котором стадией, определяющей скорость процесса, является образование разряжающейся с выделением водорода частицы ВН, образующейся из адсорбированного основания В при взаимодействии с донорами протонов, наблюдается уменьшение каталитического тока при росте отрицательного потенциала. [14]
В интервале потенциалов 1 15 - - Н 25 В основной металл обладает и большей анодной поляризуемостью и более положительными потенциалами, чем металл околошовной зоны и, следовательно, растворяется с меньшими скоростями, чем металл околошовной зоны. При более положительных потенциалах ( 1 25 В) основной металл также растворяется по механизму перепассивации, о чем свидетельствует пологий ход анодной поляризационной кривой. При этом сохраняется различие в скоростях растворения основного металла и металла околошовной зоны. Таким образом, можно сказать, что причиной появления и развития ножевой коррозии сварных соединений стали 12Х18Н10Т в меланжевых растворах, как и в азотнокислых, является облегченное протеканиг анодных процессов в околошовной зоне сварного соединения. [15]
Страницы: 1 2 3 4 5