Температурный интервал - реакция
Cтраница 1
Температурный интервал реакции на родиевых образцах еще больше сдвинут в область низших температур, и наблюдаем только второй участок кривой ( рис. 3 6), описывающий уменьшение глубины превращения с повышением температуры. Энергия активации, так же как и для никелевых образцов, равна - 5 ккал / моль. [1]
 |
Показатели синтеза с ожвжеинын слоем катализатора. [2] |
При небольшом общем температурном интервале реакции нижний предел температур ограничен необходимостью избегать отложения масел и парафина на катализаторе, чтобы не нарушать нормального состояния слоя. Опытные работы показали, что даже то небольшое количество парафина ( 1 - 2 %), которое получается в процессе, может мешать нормальному его протеканию. Верхний предел температур ограничен необходимостью избегать отложения углерода на катализаторе, которое приводит к порче последнего и расстройству процесса. [3]
 |
Показатели синтеза с ожиженным слоем катализатора. [4] |
При небольшом общем температурном интервале реакции нижний предел температур ограничен необходимостью избегать отложения масел и парафина на катализаторе, чтобы не нарушать, нормального состояния слоя. Опытные работы показали, что даже то небольшое количество парафина ( 1 - 2 %), которое получается в процессе, может мешать нормальному его протеканию. Верхний предел температур ограничен необходимостью избегать отложения углерода на катализаторе, которое приводит к порче последнего и расстройству процесса. [5]
Однако для железа и никеля в заданном температурном интервале реакции нитрирования также являются термодинамически невероятными. [6]
Каталитическая химия использует оба способа активации, но только с явным преобладанием химического способа. Поэтому она обходится такими температурными интервалами реакций и вообще такими термодинамическими параметрами, которые нельзя назвать экстремальными. [7]
Способ инициирования имеет часто решающее значение для осуществления радикальной теломеризации. Метод инициирования и природа инициатора определяют температурный интервал реакции жв значительной степени ее скорость, а в некоторых случаях и направление реакции. [8]
Наиболее важные реакции риформинга, ведущие к образованию ароматических углеводородов из нафтенов и парафинов, идут с поглощением тепла, реакции гидрокрекинга и гидрогенолиза экзотермичны, реакции изомеризации парафинов и нафтенов имеют тепловой эффект, близкий к нулю. Для углеводородов Св - С10 мольные тепловые эффекты мало зависят от молекулярной массы, причем в температурном интервале реакций риформинга ( 470 - 500 С) тепловые эффекты почти не изменяются. [9]
В качестве телогенов используют вещества, содержащие связи элемент - элемент, способные к гомо-литич. Инициирование осуществляется обычными для радикальной полимеризации методами. Способ инициирования и природа инициирующей системы определяют температурный интервал реакции, ее скорость и, в нек-рых случаях, направление. [10]
В настоящее время уже определены термодинамические свойства большинства минералов, ионов, газов, позволяющие определить изобарные потенциалы ( свободные энергии) и константы равновесия отдельных наблюдаемых и предполагаемых геохимических превращений. Однако кинетика, механизмы этих превращений изучены очень слабо. Известно, что скорость термодинамически вероятных в каком-то температурном интервале реакций растет параллельно росту температуры ( правило Оствальда), однако математического выражения этой зависимости для конкретных реакций мы не знаем. Не исключено, что при низких температурах для ряда реакций они окажутся ничтожными даже в масштабах геологического времени. Многие реакции, особенно реакции с участием органических соединений, являются каталитическими, их скорости в основном зависят or состава и типа катализатора. [11]
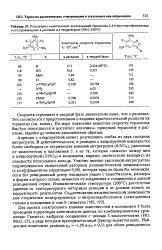 |
Результаты кинетических исследований термолиза 2 4 6-тринитрофенилазида и его производных в расплаве и в твердой фазе ( 100 С. [12] |
Априори с азндогруппой может реагировать любая из двух соседних нитрогрупп, В действительности, в реакцию с азндогруппой вовлекается более свободная от стерическнх влияний нитрогруппа ( 6 - NO2), удаленная от заместителя в положении 3, а не та, которая зажата между ним н азидогруппой ( 2 - NO2) и вынуждена, видимо, значительно выходить нз плоскости бензольного кольца. Участие именно удаленной нитрогруппы подтверждается выявленной авторами изокинетнческой зависимостью ( с коэффициентом корреляции 0 98), которая вряд лн была бы возможна, если бы реакционный центр находился рядом с заместителем, размеры н форма которого сильно меняются от соединения к соединению в данной реакционной серии. Изокинетическая температура ( 200 С) достаточно удалена от температурного интервала реакции и не должна влиять на корректность результатов. [13]
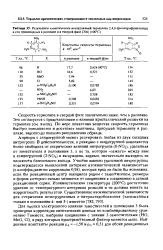 |
Результаты кинетических исследований термолиза 2 4 6-тринитрофеннлазнда и его производных в расплаве и в твердой фазе ( 100 С. [14] |
Априори с азндогруппой может реагировать любая из двух соседних нитрогрупп, В действительности, в реакцию с азндогруппой вовлекается более свободная от стерическнх влияний нитрогруппа ( 6 - NO2), удаленная от заместителя в положении 3, а не та, которая зажата между ним н азидогруппой ( 2 - NO2) и вынуждена, видимо, значительно выходить нз плоскости бензольного кольца. Участие именно удаленной яитрогруппы подтверждается выявленной авторами изокинетнческой зависимостью ( с коэффициентом корреляции 0 98), которая вряд лн была бы возможна, если бы реакционный центр находился рядом с заместителем, размеры н форма которого сильно меняются от соединения к соединению в данной реакционной серии. Изокинетическая температура ( 200 С) достаточно удалена от температурного интервала реакции и не должна влиять на корректность результатов. [15]
Страницы: 1 2