Температурный интервал - стабильность
Cтраница 1
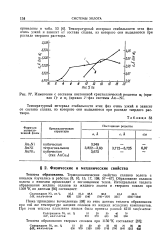 |
Изменение с составом постоянной кристаллической решетки вая / - и а2 ( кривая 2. - фаз системы Аи-Ni. [1] |
Температурный интервал стабильности этих фаз очень узкий и зависит от состава сплава, из которого они выделяются при распаде твердого раствора. [2]
Важно отметить, что данная полиморфная модификация часто может хорошо кристаллизоваться при температурах ниже своего температурного интервала стабильности, но редко кристаллизуется ( или никогда не кристаллизуется) при температурах, лежащих выше этого интервала. Видимо, это обусловлено тем, что решетке переохлажденной системы не достает подвижности для превращения; следовательно, нестабильная полиморфная модификация при температурах заметно ниже точки перехода может оказаться очень стабильной, если она сформировалась. Такой вывод свидетельствует о том, что в тех случаях, когда одна полиморфная модификация проявляет большую неустойчивость, например в случае ацетанилида, RDX, HND, система, по-видимому, является монотропной. [3]
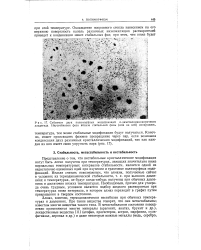 |
Сублимат двух полиморфных модификаций п-диметиламинокоричного альдегида. Неустойчивая фаза вблизи стабильной фазы ( или на ней испарилась. [4] |
Представление о том, что нестабильные кристаллические модификации могут быть легко получены при температурах, лежащих значительно ниже нормальных температурных интервалов стабильности, является одной из недостаточно оцененных идей при изучении и трактовке полиморфных модификаций. Необходимым, причем для углерода очень трудным, условием является подбор жидкого растворителя при температурах ниже интервала, в котором алмаз переходит в графит путем превращения в твердом состоянии. [5]
Конечно, этот метод получения высокотемпературных полиморфных модификаций применим только для энантиотроп-ных систем, в которых получаемая модификация имеет определенный температурный интервал стабильности. [6]
Нитрат аммония NH4NO3, традиционно но неправильно называемый аммиачной селитрой ( правильнее называть аммонийной селитрой), при атмосферном давлении в интервале от - 50 С до температуры плавления 169 6 С существует в пяти кристаллических формах / - V, различающихся структурой, удельным объемом и другими свойствами кристаллов. На политермической диаграмме системы NH4NO3 - H2O ( рис. 5.1) показаны температурные интервалы стабильности / - IV кристаллических форм. Модификация V стабильна ниже - 16 9 С. [7]
На дифрактограмме образца, нагревание которого прекращено при 485 С, преобладают линии образовавшегося по реакции (4.38) гематита, кристаллизация которого сопровождается экзотермическим эффектом при 440 С. Форма кривой ТВА указывает на то, что выделение серосодержащих газов начинается непосредственно после завершения дегидратации, т.е. отсутствует выраженный температурный интервал стабильности в составе продуктов обжига. Развиваются основной ( уравнение (4.6)) и сопутствующие процессы диссоциации сульфата FeS04 и восстановления оксидов. [8]
Таким образом, на процессы образования и стабилизации т-фаз оказывает влияние как размерный, так и электронный фактор, причем в одних случаях преобладающее значение имеет первый фактор, а в других - второй. Имеются экспериментальные данные, подтверждающие важную роль обоих факторов. Здесь следует отметить, например, появление а-фаз в тройных системах в тех случаях, когда они не существуют ни в одной из двойных систем, образующих данную тройную. Температурный интервал стабильности некоторых а-фаз уменьшается при увеличении отношения атомных радиусов компонентов, но может расширяться при добавлении третьего компонента. [9]
Таким образом, на процессы образования и стабилизации г-фаз оказывает влияние как размерный, так и электронный фактор, причем в одних случаях преобладающее значение имеет первый фактор, а в других - второй. Имеются экспериментальные данные, подтверждающие важную роль обоих факторов. Здесь следует отметить, например, появление а-фаз в тройных системах в тех случаях, когда они не существуют ни в одной из двойных систем, образующих данную тройную. Температурный интервал стабильности некоторых а-фаз уменьшается при увеличении отношения атомных радиусов компонентов, но может расширяться при добавлении третьего компонента. [10]
Согласно Уовнеру [38], при температурах выше 894 К волокна бора теряют стабильность. Уовнер приводит данные Джиллеспи, показавшего, что уже при коротких ( 15 мин) выдержках при 1227 К наблюдается рост зерен ромбоэдрического ( 3-бора. Уовнер обсуждает также аналогичные данные Липситта, отметившего, кроме того, возможность структурных изменений бора в интервале температур 977 - 1033 К в атмосфере хлористого водорода и хлора. В глубинных слоях волокон ( после удаления поверхностного слоя) структурные изменения не были обнаружены, что согласуется с уравнением Клауэиуса - Клапейрона для реакций, протекающих с увеличением объема. Если исключить из состава композита следы таких катализаторов, как хлор, и предотвратить объемные изменения, то температурный интервал стабильности волокон в титановой матрице должен увеличиться. [11]
Страницы: 1