Классическая энергия - активация
Cтраница 1
Классическая энергия активации, вычисленная в предположении, что кулоновская энергия составляет 14 / 0 энергии связи двухатомных молекул, найдена равной 48 3 ккал. [1]
А, соответственно; классическая энергия активации Екл, согласно сказанному, не зависит от массы изотопов и поэтому из выражения (12.68) выпадает. [2]
При всякой химической реакции преодолевается потенциальный барьер, минимальное значение которого - классическая энергия активации - связано с наиболее вероятными состояниями реагирующей системы. [3]
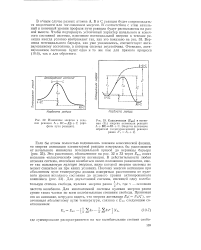
Это расстояние, обозначенное на рис. 32 и 33 через Екл, носит название классической энергии активации. В действительности любая атомная система, способная колебаться около положения равновесия, имеет так называемую нулевую энергию, ниже которой энергия системы не может снизиться ни при каких условиях. [5]
Заметим, что в уравнении (10.9) и в последующих формулах настоящего параграфа речь, очевидно, идет о классической энергии активации. [6]
Как видно, реагирующая система, прежде чем перейти в конечное состояние, должна преодолеть потенциальный барьер, равный Ека классической энергии активации. [7]
Предполагая, что 17 / 0 энергии связи составляет кулоновская энергия, и пренебрегая нулевой энергией, можно было найти классическую энергию активации, которая оказалась равной 53 ккал. В предположении 20 / 0 кулоновской энергии, для Ес получается значение 43, 6 ккал. [8]
Как видно, реагирующая система, прежде чем перейти к конечному состоянию, должна преодолеть потенциальный барьер, равный ЕКЛ - классической энергии активации. Разность между потенциальными энергиями исходных веществ и продуктов реакции равняется тепловому эффекту Q - ДЯ. [9]
 |
Классическая Екя и истинная Е0 энергии активации реакции XY Z - X YZ [ энергия активации обратной ( эндотермической реакции равна EQ EO Q ]. [10] |
Как видно, реагирующая система, прежде чем перейти к конечному состоянию, должна преодолеть потенциальный барьер, равный кл - классической энергии активации. Разность между потенциальными энергиями исходных веществ и продуктов реакции равняется тепловому эффекту Q - ДЯ. [11]
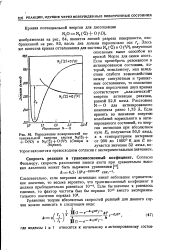 |
Пересечение поверхностей по - нУле Ео получается 50 0 ккал, тенциальной энергии систем К Ч. - - 0 ( Ш и N2 (. S 0 ( 3P ( Стирн и Эйринг. [12] |
Если пренебречь резонансом в активированном состоянии, который, невидимому, мал вследствие слабого взаимодействия между сингулетным и триплет-ным состояниями, то положение точки пересечения двух кривых соответствует классической энергии активации реакции, равной 52 8 ккал. Расстояние N - О для активированного комплекса равно 1 73 А. [13]
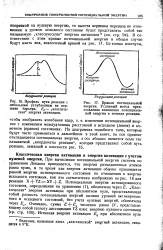 |
Профиль пути реакции с небольшим углублением на вершине барьера. Ее -. классическая энергия активации. [14] |
При вычислении потенциальной энергии системы по уравнению Лондона принимается, что энергия разъединенных атомов равна нулю, в то время как энергия активации обычно принимается равной энергии активированного состояния по отношению к энергии исходного состояния, как это схематически изображено на рис. 18 для реакции X - ] - YZ XY - - Z. Классическая энергия активации при абсолютном нуле, представляющая собой разность потенциальных энергий низших уровней активированного и исходного состояний, без учета нулевых энергий, обозначена через Ес. Очевидно, сумма Е - - Ее численно равна D, представляющему собой теплоту диссоциации YZ плюс энергию нулевого состояния ( ср. [15]
Страницы: 1