Термодинамическая интерпретация
Cтраница 1
Термодинамическая интерпретация Е существенно различна для сжимаемой и для несжимаемой жидкости: эти случаи соответственно будут рассматриваться отдельно. [1]
Заметим, что термодинамическая интерпретация е существенно различна для сжимаемой и несжимаемой жидкости. [2]
Это соотношение дает простую термодинамическую интерпретацию К. [3]
Наш анализ не представляет только термодинамическую интерпретацию уравнения Шеннона. Он приводит к выводу, что представления кибернетики не могут быть вполне отвлечены от структуры мышления, но заранее предполагают ее некоторые общие свойства. Это станет ясно, если ближе проанализировать содержание работы информации. Для этого разберем четыре термодинамических модели, две из которых отвечают акту получения информации, третья выражает особый не шенноновский вид информации, а четвертая относится к переходу от информации к мышлению в его простейшей и вместе с тем важнейшей логической ( дискурсивной) форме. [4]
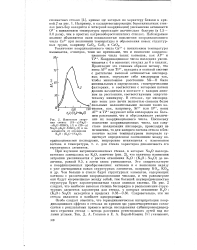 |
Изменение энтропии стекол ( 18 -. r Na20 iK2O - 82Si02 ( 7 и ( 28 - 1 / Na20 -. / K20 - 72Si02 ( 2 в зависимости от отношения К2О. ( K20 Na2O. [5] |
Особо следует отметить, что термодинамическая интерпретация координационного эффекта в стеклах по кривым эдс удовлетворительно согласуется с результатами прямого метода исследования субмикронеоднород-ного строения стекол - метода рассеяния рентгеновских лучей под малыми углами. [6]
Это выражение может служить в качестве термодинамической интерпретации статистической суммы. [7]
Однако в этом случае вопрос о термодинамической интерпретации функционала S и параметров г / - вдали от равновесия остается открытым [ 19, гл. [8]
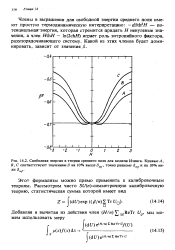 |
Свободная энергия в теории среднего поля для модели Изинга. Кривые Л, В, С соответствуют значениям 0 на 10 % выше mf, точно равному & mf и на 10 % ниже / 3. [9] |
Члены в выражении для свободной энергии среднего поля имеют простую термодинамическую интерпретацию: - df3th2H - по-тенциальная-энергия, которая стремится придать Н ненулевые значения, а член HthH - ln ( 2ch / /) играет роль энтропийного фактора, разупорядочивающего систему. [10]
Все перечисленные законы открыты экспериментально и уже после этого получили термодинамическую интерпретацию. [11]
Следует напомнить об условиях ( VIII-26), связанных с термодинамической интерпретацией кинетического уравнения. [12]
Следует напомнить об условиях ( VIII-26), связанных с термодинамической интерпретацией кинетического уравнения. [13]
Поскольку основой газохроматографической идентификации являются величины удерживания, первая глава посвящена их классификации, термодинамической интерпретации, а также рассмотрению основных факторов, вызывающих погрешности при их определении. В двух последующих главах описывается влияние природы молекул и физико-химических свойств сорбатов и неподвижных фаз на хроматографическое удерживание и приводятся различные корреляции, которые могут использоваться для качественного анализа. Концепция хроматографического спектра и методы использования его для групповой, а в некоторых случаях и для индивидуальной идентификации неизвестных соединений рассмотрены в четвертой главе. [14]
Поскольку фазовые равновесия имеют большое значение в физической химии силикатов, необходимо, несмотря на наличие хорошо разработанной литературы по этому вопросу [17, 43, 136], хотя бы вкратце познакомиться с термодинамической интерпретацией правила фаз и его приложениями к силикатным системам. Без ясного понимания фазовых диаграмм равновесного сосуществования различных твердых и жидких фаз в силикатных системах нельзя правильно разобраться в существе протекающих в них физико-химических процессов. Правило фаз дает возможность определять условия, при которых в равновесной системе сохраняется сосуществующее число фаз. Уравнение фаз устанавливает математическую связь между числом степеней свободы, числом компонентов и числом фаз в данной равновесной системе. [15]
Страницы: 1 2 3