Выделение - кристалл - соль
Cтраница 1
Выделение кристаллов солей из раствора представляет собой двухступенчатый процесс: сначала образуются центры кристаллизации, а затем происходит рост кристаллов. Главным процессом, определяющим интенсивность выделения солей из пересыщенного раствора, является процесс зарождения кристаллов. [1]
Поэтому при чрезмерном повышении температуры электролиза в ваннах происходит выделение кристаллов соли, которые забивают поры диафрагмы, что приводит к нарушению нормального хода процесса. [2]
Если вынести кипение раствора за пределы поверхности нагрева, то выделение кристаллов соли произойдет в этой зоне, и, следовательно, скорость инкрустации греющих трубок значительно уменьшится. [3]
Впервые они были всесторонне охарактеризованы при изучении структурно-механических свойств систем типа - консистентных смазок [43], получаемых при выделении волокнистых кристаллов солей жирных кислот из пересыщенных растворов в углеводородных жидкостях. Все высокодисперсные поликристаллические материалы - большинство металлов и сплавов, многие горные породы, а также искусственные строительные камни - представляют собой кристаллизационные структуры. [4]
При охлаждении рассола с концентрацией больше, чем в криогидратной точке, например 25 %, концентрация раствора остается постоянной до достижения температуры, соответствующей точке Ь, при которой начнется выделение кристаллов соли. [5]
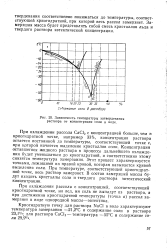 |
Зависимость температуры затвердевания раствора от концентрации соли в воде. [6] |
При охлаждении рассола СаС12 с концентрацией больше, чем в криогидратной точке, например 33 %, концентрация раствора остается постоянной до температуры, соответствующей точке с, при которой начнется выделение кристаллов соли. [7]
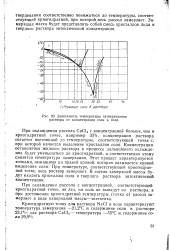 |
Зависимость температуры затвердевания раствора от концентрации соли в воде. [8] |
При охлаждении рассола СаС12 с концентрацией больше, чем в криогидратной точке, например 33 %, концентрация раствора остается постоянной до температуры, соответствующей точке с, при которой начнется выделение кристаллов соли. [9]
 |
Схема выпарной установки смешанного типа. [10] |
При необходимости выделения твердой фазы из растворов кон - 1ентрацией, близкой к насыщению, исходный раствор обычно полется одновременно во все корпуса многокорпусной установки и шпаривается при постоянной концентрации с выделением кристаллов соли за счет удаления части растворителя при кипении. Вторичный пар, полученный при кипении раствора в выпарном аппарате, направляется на обогрев следующего корпуса. [11]
Наряду с ними в практике кристаллизации из растворов иногда используют кристаллизацию высаливанием ( введение в раствор веществ, понижающих растворимость соли), вымораживанием ( охлаждением растворов до отрицательных температур с выделением кристаллов соли или их концентрирование удалением части растворителя в виде льда) или за счет химической реакции, обеспечивающей пересыщение раствора а также высокотемпературную ( автоклавную) кристаллизацию, обеспечивающую возможность получения кристаллогидратов с минимальным содержанием кристаллизационной влаги. [12]
Кипение раствора начинается в зоне выше поверхности нагрева, где давление движущегося раствора снижается до давления насыщения. Так как выделение кристаллов соли происходит в зоне кипения раствора, то поверхность нагрева выпарного аппарата при этом длительное время остается чистой. Правда, полностью избежать отложения кристаллов солей на поверхности нагрева при этом не удается из-за местного перегрева в тонком ламинарном слое и появления зародышей кристаллов на стенке; но скорость инкрустации значительно уменьшается. [13]
Для любых растворов с концентрацией KNO3 выше 11 62 % при охлаждении сначала выделяются кристаллы нитрата калия. При дальнейшем охлаждении по мере выделения кристаллов соли концентрация ее в остающемся жидком растворе понижается. Так протекает процесс, пока не достигается эвтектическая температура. При этой температуре ( при дальнейшем отнятии теплоты) остающийся раствор замерзает полностью в виде криогидрата того же состава. [14]
В случае применения проточных датчиков при измерениях рН концентированных солевых растворов возникает опасность увеличения поверхностной проводимости. Как известно, насыщенные растворы хлористого натрия, калия и других ратворов обладают свойствами ползучести по микрокапиллярным трещинам с выделением кристаллов соли на поверхности. [15]
Страницы: 1 2