Выделение - бактерия
Cтраница 1
Выделение бактерий из различных органов растений - листьев, корней, семян и др. - требует дифференцированного подхода. [1]
Для выделения бактерий группы coli-aerogenes методом прямого посева Киченко ( 1942) рекомендует применять МП А с желчью и розоловой кислотой. На этой среде хорошо задерживается рост сапрофитных бактерий нефекального происхождения. Микроорганизмы же группы кишечной палочки на ней прекрасно размножаются. Мы обычно работали с этой средой. [2]
Методы выделения термофильных и мезофиль-ных бактерий в основном сходны. Различие заключается лишь в температуре выращивания. Для того чтобы точно установить оптимальную температуру развития и закрепить ее, культуру необходимо длительно ( 1 - 2 месяца) пассировать ( пересевать) в диапазоне найденного оптимума. [3]
Если поражены проводящие сосуды, то для выделения бактерий отбирают участки с начальными признаками поражения, изм ( льчают их и высевают на питательную среду. [4]
Среда № 5 ( висмутсульфит агар сухой) - для выделения бактерий семейства Enterobacteriaceae - готовят согласно прописи на этикетке. [5]
Среда № 4 ( агар Эндо сухой) - для выделения бактерий семейства Enterobacteriaceae - готовят согласно прописи на этикетке. [6]
Среда № 5 ( висмутсульфит агар сухой) - для выделения бактерий семейства Enterobacteriaceae - готовят согласно прописи на этикетке. [7]
Напряженность антагонистических взаимоотношений среди микробов, населяющих почву, была использована человеком с цилью выделения бактерий, продуцирующих различные антибиотические средства. [8]
Так как техника обнаружения ряда бактериофагов, например дизентерийных и брюшно-тифозных, более проста и надежна, чем методика выделения соответствующих бактерий, то использование бактериофага в качестве санитарно-показатель-ного микроорганизма имеет большие перспективы. Особенно целесообразным представляется использование бактериофагов как показателей фекального загрязнения воды в тех случаях, когда имеется опасность передачи через воду вирусных инфекций. Вирусы-возбудители полиомиелита, эпидемического гепатита и некоторых других заболеваний, передающихся через воду, выживают в воде и почве дольше, чем кишечная палочка. Поэтому, когда появляется опасность возникновения подобных вирусных эпидемий, бактериофаги, которые по своей устойчивости более близки к вирусам, могут быть использованы как санитарно-показательные микроорганизмы, имеющие преимущество перед кишечной палочкой. [9]
Систематика бактерий проводится на основании определенных признаков у группы микроорганизмов. Для выделения бактерий в определенную систематическую группу необходимо тщательное изучение морфологии, способности к перемещению, спорообразованию. Отличительным признаком служит отношение клеток к окрашиванию. Наиболее употребительным методом дифференциации клеток микроорганизмов является окрашивание по Граму. Сущность этого метода заключается в выяснении возможности удерживания клеткой красителя ( кристаллический фиолетовый - иод) при последующей обработке препарата спиртом. Использование этого индикаторного метода позволяет выделить две группы микроорганизмов: грамположительные, сохраняющие окраску; и грамотрица-тельные, обесцвечивающиеся при обработке препарата спиртом. [10]
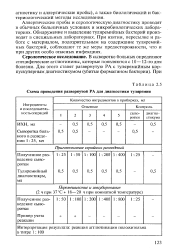 |
Схема проведения развернутой РА для диагностики туляремии. [11] |
Аллергические пробы и серологическую диагностику проводят в обычных больничных условиях и микробиологических лабораториях. Обнаружение и выделение туляремийных бактерий производят в специальных лабораториях. При взятии, пересылке и работе с материалом, подозрительным на содержание туляремийных бактерий, соблюдают те же меры предосторожности, что и при других особо опасных инфекциях. [12]
Большинство производственных процессов сопровождается выделением в воздух рабочих помещений вредных для здоровья человека газов и паров. Кроме того, некоторые процессы сопровождаются выделением большого количества теплоты, водяных паров, пыли, в результате чего в помещении повышаются температура воздуха, влажность, запыленность, загазованность. В отдельных производственных помещениях ( помещения для содержания животных, птиц) технологический процесс сопровождается выделением вредных бактерий. При длительном пребывании большого количества людей в закрытых помещениях ( цехи, зрительные залы) повышаются температура и влажность воздуха, увеличивается содержание углекислого газа, а количество кислорода уменьшается. [13]
Видовой и родовой состав бактерий активного ила весьма разнообразен. Важной задачей при его изучении является правильный подбор питательных сред, из которых каждая в отдельности не может обеспечить рост всех обитателей активного ила. В связи с этим были предприняты попытки изучить пищевые потребности микроорганизмов. Дайэс и Бхэт [342] нашли, что только 24 % из ПО изолятов, полученных из необработанных сточных вод, и 8 % из 150 штаммов, выделенных из активного ила, не нуждаются ни в витаминах, ни в аминокислотах при росте на среде, содержащей глицерин, сукцинат натрия и нитрат аммония. Эффективность экстракта зависит от источника и образца активного ила. Более половины из 127 штаммов, выделенных на среде с экстрактом активного ила, не росли на синтетических средах с глюкозой, аминокислотами, витаминами, дрожжевым экстрактом и минеральными солями. В то же время другие исследователи [481] для выделения бактерий из сточной и речной воды как наиболее пригодную среду рекомендуют казеино-пептоно-крахмальный агар. Однако на других семи средах, использованных в опытах, в том числе приготовленных на основе загрязненных вод, получены сходные результаты. Для количественного учета микрофлоры большое значение имеет гомогенизация активного ила перед посевом на питательные среды. [14]
Страницы: 1