Выделение - металл
Cтраница 4
Для выделения металлов на электродах обычно используется платиновый или ртутный электрод. Потенциал, при котором производится осаждение, регулируют или вручную или с применением специальных электронных приборов - потенциостатов. [46]
Для выделения металлов, которые не выделяются электролизом при обычных условиях. [47]
Практически выделение металла можно считать законченным, если остаточная концентрация его составит 10 - 4 - 10 - 5 % от исходной. Такому изменению концентрации соответствует сдвиг потенциала разряда в отрицательную сторону на 0 24 - 0 36 в для металлов, дающих однозарядные ионы, и на 0 12 - 0 18 s для металлов с двузарядными ионами. Поэтому считают, что минимальное численное значение разницы в потенциалах разряда, обеспечивающее беспрепятственное раздельное определение металлов при их совместном присутствии, должно равняться 0 4 в при однозарядных и 0 2 в при двузарядных ионах. При этом необходимо, чтобы в течение всего времени выделения металла плотность тока не превышала предельного значения. [48]
Практически выделение металла можно считать законченным, если остаточная концентрация его составит 10 - 4 - 10 - 6 % от исходной. Такому изменению концентрации соответствует сдвиг потенциала разряда в отрицательную сторону на 0 24 - 0 36 в для металлов, дающих однозарядные ионы, и на 0 12 - 0 18 в для металлов с двухзаряд-ными ионами. Поэтому считают, что минимальное численное значение разницы в потенциалах разряда, обеспечивающее беспрепятственное раздельное определение металлов при их совместном присутствии, должно равняться 0 4 в при однозарядных и 0 2 в при двухзарядных ионах. [49]
 |
Изменение концентрации разряжающегося иона в диффузионном слое у катода. [50] |
Если выделение металла сопровождается выделением водорода, то образуются очень непрочные порошкообразные или губчатые осадки. [51]
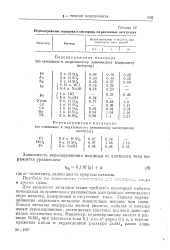 |
Перенапряжение водорода и кислорода на различных электродах. [52] |
Для выделения металлов также требуется некоторый избыток потенциала по сравнению с равновесным электродным потенциалом этого металла, измеряемым в отсутствие тока. Однако перена-пр яжение выделения металлов значительно меньше, чем газов. Только металлы подгруппы железа ( железо, кобальт и никель) имеют перенапряжение, достигающее заметных величин даже при малых плотностях тока. [53]
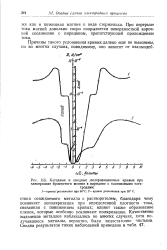 |
Катодные и анодные поляризационные кривые при электролизе бромистого магния в пиридине с платиновыми электродами. [54] |
Качественно выделение металлов наблюдалось во многих случаях, хотя получавшиеся металлы, вероятно, были недостаточно чистыми. [55]
Если выделение металла совершается на твердом катоде, то в результате разряда ионов образуются первоначально адатомы ме-тллла ( или его адионы), которые лишь на следующей стадии переходят в решетку твердого металла. [56]
Для выделения металлов, электродные потенциалы которых намного отрицательнее водорода или на которых водород выделяется без перенапряжения, применить электролиз водных растворов нельзя. Многие из этих металлов способны вытеснять водород из воды. К числу металлов, которые не могут быть получены электролизом водных растворов, относятся следующие: Li, Na, К, Rb, Cs, Ca, Sr, Ba, Be, Mg, Al, Ti, Zr, Hf, Th, U, Nb, Та, Mo, W, а также все лантаноиды и актиноиды. Все эти металлы могут быть получены электролизом солевых расплавов, получивших название ионных расплавов. [57]
Для выделения металла из раствора его комплексного соединения требуется наложить более высокий потенциал, чем в отсутствие комплексообразующего лиганда. Величину сдвига потенциала легко рассчитать по константе образования комплекса. Данные, представленные в табл. 19 - 1, показывают, что изменения потенциала могут быть весьма значительными и должны приниматься во внимание при рассмотрении возможности электролитического-определения или разделения элементов. Так, например, в кислом растворе медь можно легко отделить от цинка или кадмия, тогда как в присутствии заметных количеств цианид-ионов наблюдается одновременное выделение всех трех металлов. Более значительный сдвиг потенциала для серебра или меди ( табл. 19 - 1) объясняется большей устойчивостью их цианидных комплексов. [58]
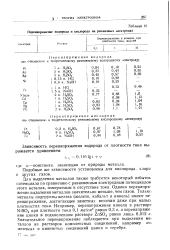 |
Перенапряжение водорода и кислорода на различных электродах. [59] |
Для выделения металлов также требуется некоторый избыток потенциала по сравнению с равновесным электродным потенциалом этого металла, измеряемым в отсутствие тока. Однако перенапряжение выделения металлов значительно меньше, чем газов. Только металлы подгруппы железа ( железо, кобальт и никель) имеют перенапряжение, достигающее заметных величин даже при малых плотностях тока. Например, перенапряжение никеля в растворе NiSO4 при плотности тока 0 1 ма / см равно 0 3 в, а перенапряжение цинка в подкисленном растворе ZnSO4 равно лишь 0 012 в. Значительное перенапряжение наблюдается при выделении металлов из растворов комплексных соединений, например аммиачных и цианистых соединений цинка и серебра. [60]
Страницы: 1 2 3 4 5