Выделение - бериллий
Cтраница 1
Выделение бериллия в количестве от 0 0005 г ( в расчете на ВеО) и менее требует более длительного отстаивания ввиду медленного выделения осадка в мелкокристаллической форме. [1]
Выделение бериллия из облученного лития проводят способом, описанным на стр. [2]
 |
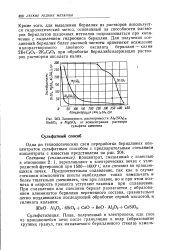
Коэффициенты распределения D Be, Mg и А1 на смоле Dowex 1 - X8 в водно-органической среде, содержащей ( в об. % 90 органического растворителя, 10 азотной или соляной кислоты. [3] |
Для выделения бериллия из водных или кислых растворов анионооб-менники используются в меньшей степени по сравнению с катионообменни-ками. Следовательно, он практически не поглощается во всем интервале концентраций соляной или азотной кислот. В табл. 5.14 для сравнения приведены значения коэффициентов распределения алюминия и магния. [4]
Высокий потенциал выделения бериллия позволяет количественно отделять его от многих металлов на платиновом [697- 701] или ртутном [702-707] катодах. [5]
 |
Зависимость растворимости A12 ( SO4 3. [6] |
Кроме того, для выделения бериллия из растворов используется гидролитический метод, основанный на способности растворов бериллатов щелочных металлов гидролизоваться при кипячении с выделением гидроокиси бериллия. Для получения соединений бериллия более высокой чистоты применяют осаждение малорастворимого двойного оксалата бериллия - калия 2ВеС2О4 2К2С2О4 при обработке бериллийсодержащих растворов раствором оксалата калия. [7]
Наиболее распространенный способ очистки и выделения бериллия из сульфатных растворов основан на неспособности бериллия, в отличие, от алюминия, образовывать квасцы и на низкой растворимости алюминиево-аммонийных квасцов в растворе сульфатов бериллия и аммония. [8]
Их можно определить в фильтрате после выделения бериллия, разумеется, после разрушения комплексона. [9]
Ионообменные методы представляют значительный интерес для выделения бериллия из растворов, содержащих большие количества других металлов. Согласно Шуберту, Линденбауму и Вест-фалю [68] в кислой среде бериллий образует с сульфосалициловой кислотой незаряженные комплексы. Чтобы отделить бериллий от ионов кальция, меди и уранила, ионы металлов из хлоридного раствора поглощают сульфокатионитом. [10]
Это может быть сделано в фильтрате после выделения бериллия, разумеется после разрушения комплексона. [11]
В настоящее время не существует прямых методов выделения бериллия, позволяющих за одну операцию отделять его от большинства элементов. Для выделения бериллия из большинства материалов, по-видимому, следует комбинировать несколько методов. [12]
Современные методы отделения бериллия от мешающих определению элементов базируются на выделении бериллия в виде труднорастворимых соединений в присутствии трилона Б, играющего роль маскирующего ком-плексообразователя. Успешное отделение бериллия практически от всех сопутствующих ему элементов достигается при осаждении его в виде гидроокиси, фосфата, а еще лучше - арсената; при выделении малых количеств применимы и описанные выше органические осадители. [13]
Во время проведения исследований появилась работа Дема [25], который рекомендует выделение бериллия в виде коричнокислой соли, не имеющей постоянного состава. [14]
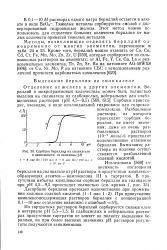 |
Сорбция берилли на силикагеле в зависимости от величины рН. [15] |
Страницы: 1 2 3