Выделение - реакционное тепло
Cтраница 1
Выделение реакционного тепла, пропорционального количеству прореагировавших веществ, делает возможным определение протяженности зоны реакции по изменению температуры ДХЭ по высоте реактора. Уровень, на котором прекращается рост температуры, соответствует полной утилизации хлора из ДХЭ, то есть верхней границе зоны реакции. [1]
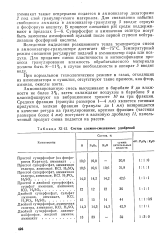 |
Состав сложно-смешанных удобрений. [2] |
Вследствие выделения реакционного тепла температура смеси в аммонизаторе-грануляторе достигает 60 - 75 С. Температурный режим смешения регулируют подачей в аммонизатор пара или воздуха. Для придания смеси пластичности и интенсификации процесса гранулирования влажность обрабатываемого материала должна быть 8 - 11 %, в случае необходимости в аппарат 5 вводят воду. [3]
 |
Схема производства сложно-смешанных удобрений. [4] |
Вследствие выделения реакционного тепла температура смеси в аммонизаторе достигает 60 - 75 С. [5]
Температура, необходимая для проведения синтеза NH3, достигается путем предварительного подогрева азото-водо-родной смеси и за счет выделения реакционного тепла. [7]
Таким образом, обогащение воздушного дутья кислородом приводит к уменьшению общего объема газа с образованием такого же количества СО и одинаковым выделением реакционного тепла, как и без добавления СЬ. Следовательно, процесс протекает при более высокой температуре реакции восстановления ( более горячий ход генератора) и достигается большая интенсивность газификации. [8]
В хлораторе бензола кроме образования ХБ и ДХБ происходят: растворение РеС13 и хлора в бензоле, испарение бензола ( вследствие выделения реакционного тепла), десорбция НС1, взаимодействие хлора с железом с образованием FeCU. Большинство этих процессов массообменные; для их ускорения в реакторе должны возможно тщательнее смешиваться газ с жидкостью и осуществляться интенсивный контакт газо-жидкостной эмульсии с железом. [9]
Процесс считается законченным, когда снижение давления водорода в автоклаве замедлится ( в течение процесса гидрирования давление поддерживают периодическим дополнением водорода из баллона) и выделение реакционного тепла прекратится. Тогда автоклав охлаждают до 40 и продувают азотом, после чего реакционную массу нейтрализуют содой. [10]
У большинства реакций скорость наибольшая в начале процесса, а затем по мере израсходования сырья она уменьшается. Соответственно изменяется и выделение реакционного тепла. Автокаталитические реакции и реакции с последовательными стадиями идут сначала с нарастающей скоростью, которая достигает максимума и затем снижается. Скорость выделения тепла следует той же закономерности. [11]
По теории Зволинского и Эйринга допускается, что теплота реакции полностью расходуется на нагрев поверхности раздела металл - окись. Но в реакции окисления, где реагенты должны проходить через слой окиси, участки, которые нагреваются за счет выделения теплоты реакции, могут быть также на поверхности раздела окись - газ, а иногда даже в окиснем слое. Всегда ли учитывается влияние места выделения реакционного тепла на воспламенение. [12]
При обычных температурах в темноте хлор и водород не взаимодействуют. На свету или при нагревании реакция в смеси этих газов сопровождается взрывом. Спокойное протекание реакции между хлором и водородом ( без взрыва) возможно при непрерывном поступлении газов в реакционную зону и высокой температуре ( обычно 2000 - 2400 С), которая поддерживается за счет выделения реакционного тепла. Реагирующие газы образуют светящийся факел бледно-лунного цвета. [13]
При обычных температурах в темноте хлор и водород не взаимодействуют. На свету или при нагревании реакция в смесл этих газов сопровождается взрывом. Спокойное протекание реакции между хлором и водородом ( без взрыва) возможно пои непрерывном поступлении газов в реакционную зону и высокой температуре ( обычно 2000 - 2400 С), которая поддерживается за счет выделения реакционного тепла. Реагирующие газы образуют светящийся факел бледно-лунного цвета. [14]
Страницы: 1