Выделение - дейтерий
Cтраница 1
Выделение дейтерия из водорода методом глубокого охлаждения основано на процессе ректификации. [1]
Перенапряжение выделения дейтерия на катоде больше примерно на 0 1 в, чем протия, а стандартный потенциал дейтерия на 0 003 в электроотрицательнее, чем протия. Поэтому при электролизе дейтерий переходит в газовую фазу в относительно меньших количествах, чем, протий, вследствие чего жидкая фаза обогащается тяжелой водой. [2]
При осуществлении процесса выделения дейтерия из водорода методом низкотемпературной дистилляции исключительно важное значение приобретает проблема очистки сырьевого водорода от примесей, которые при охлаждении затвердевают и могут нарушить нормальную работу теплообменных аппаратов и ректификационной колонны. Для нормальной работы колонны разделяемый водород должен быть очищен до остаточного содержания примесей порядка 10 8 - 10 - 7 доли по объему. Таким образом, к очистке предъявляются весьма высокие требования. [3]
Так как перенапряжение выделения дейтерия на катоде примерно на 0 1 В выше, чем протия, при электролитическом разложении Природной воды происходит постепенное обогащение жидкой фазьг дейтерием. Электролитическим путем тяжелая вода впервые была получена в 1932 г. в США Льюисом, а в СССР в 1934 г. Бродским. [4]
В книге излагаются физико-технические основы выделения дейтерия из водорода методом глубокого охлаждения. В основу книги положен личный опыт авторов; также широко использованы советские и зарубежные публикации. [5]
 |
Схема выделения дейтерия из электролизного водорода с использованием. [6] |
Ниже рассматривается несколько типов разработанных схем для выделения дейтерия из сырья различного качества. [7]
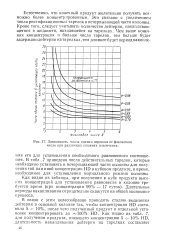 |
Зависимость числа единиц переноса от флегмового числа при различных степенях извлечения. [8] |
В связи с этим целесообразно проводить стадию выделения дейтерия в основной колонне так, чтобы концентрация HD составила 5 - ч - 10 %, после чего полученный продукт в отдельной установке концентрировать до - 100 % HD. [9]
Ввиду большой значимости разделения изотопов, и в частности выделения дейтерия, было экспериментально изучено большое число различных методов. [10]
Для получения дейтерия необходима определенная концентрация соединения НД и затем, выделение дейтерия. [11]
Наибольшее значение достигается в условиях электролиза, при которых скорость реакции выделения дейтерия опережает скорость реакции изотопного обмена. В связи с этим электролиз рекомендуют проводить при высоких катодных плотностях тока, пониженных температурах и с использованием катодов, материал которых оказывает минимальное каталитическое действие на реакцию изотопного обмена. [12]
В разных странах было проведено очень много работ по изысканию методов выделения дейтерия, но только немногие из них оказались экономически выгодными в промышленном масштабе. [13]
Наибольшее значение а достигается в условиях электролиза, при которых скорость реакции выделения дейтерия опережает скорость реакции изотопного обмена. В связи с этим электролиз рекомендуют проводить при высоких катодных плотностях тока, пониженных температурах и с использованием катодов, материал которых оказывает минимальное каталитическое действие на реакцию изотопного обмена. [14]
Вполне очевидно, что добавочное напряжение, необходимое для выделения из комплекса HSO обычного водорода, будет меньше, чем для выделения дейтерия, а поэтому обычный водород будет выделяться легче, чем дейтерий. [15]
Страницы: 1 2 3