Электролитическое выделение - медь
Cтраница 1
Электролитическое выделение меди осуществляется в ваннах с нерастворимыми анодами. [1]
Электролитическое выделение меди из растворов от регенерации катализатора СК, Отч. [2]
Электролитическое выделение меди и цинка из хлористых растворов, Отч. [3]
Реэкстрагируют медь отработанным электролитом этделения электролитического выделения меди. [4]
Остюда видно также, что при электролитическом выделении меди ионы железа ( III) мешают, так как они восстанлвливаются раньше ионов меди и концентрация их в растворе не изменяется из-за окисления ионов железа ( II) на аноде. [5]
Отсюда видно также, что при электролитическом выделении меди ионы железа ( 1Щ мешают, так как они восстанавливаются раньше ионов меди и концентрация их в растворе не изменяется из-за окисления ионов железа ( II) на аноде. [6]
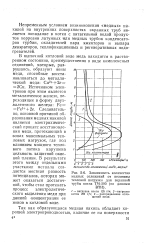 |
Зависимость количества медных отложений от величины. [7] |
РУбы котла: 2 - 00 ( по данным процесс электролитического выделения меди при данной ( концентрации ее ионов в котловой воде. [8]
При этом значении потенциала осаждение цинка не начнется, поэтому на вопрос о возможности электролитического выделения меди в присутствии цинка из сернокислых растворов следует отвечать утвердительно. [9]
Окись цинка является более электроположительной фазой, чем сульфид цинка, поэтому такое покрытие должно способствовать уменьшению электролитического выделения меди и цинка. [10]
Избирательное выделение меди достигается обработкой органической фазы эквивалентным количеством серной кислоты, причем в одну ступень могут быть получены насыщенные растворы сульфата меди, пригодные для кристаллизации соли или электролитического выделения меди. [11]
Определение никеля и цинка по ГОСТу [1] является длительным и весьма трудоемким. После электролитического выделения меди осаждают никель в виде диметилглиоксимата, а в фильтрате после отделения никеля определяют цинк в виде фосфата. На определение никеля и цинка по ГОСТу требуется 8 - 12 часов. [12]
Лучшие результаты дает метод с предварительным электролитическим выделением меди [100], последующей экстракцией иодида мышьяка ( III) хлороформом и определением его в виде мышьяковомолибденовой сини. По другому варианту, пробу растворяют в смеси хлористоводородной кислоты и пергидроля, избыток последнего удаляют кипячением и восстановлением гипофосфитом [101, 102], а затем экстрагируют хлорид мышьяка ( III) и продолжают определение, как и в первом варианте. Этот метод дает удовлетворительные результаты. [13]
Навеску меди растворяют в азотной кислоте. Если медь определяют электролизом, то после ее выделения оставшееся в растворе железо окисляют перманганатом, так как при электролитическом выделении меди трехвалентное железо переходит в двухвалентное. Железо определяют роданидным методом. Если же медь не определяют, то железо осаждают аммиаком вместе с алюминием ( применяют как коллектор) в виде гидроокиси, после чего осадок растворяют в азотной кислоте ( 1: 1) и определяют железо ( см. стр. [14]
Следовательно, основной причиной образования накипей является электрохимический процесс восстановления меди, протекающий в зонах максимальных тепловых нагрузок, где под влиянием мощного теплового потока нарушена цельность защитной окисной пленки. В результате этого между отдельными участками металла создается местная разность потенциалов, которая может оказаться достаточной, чтобы стал протекать процесс электролитического выделения меди при данной концентрации ее ионов в котловой воде. Так как образующаяся медная накипь обладает хорошей электропроводностью, наличие ее на поверхности нагрева не является существенной помехой для продолжения электрохимических процессов, в результате которых выделяются новые порции металлической меди. [15]
Страницы: 1 2