Совместное выделение
Cтраница 2
Линия совместного выделения КА1С14 и твердых растворов экстремумов не имеет. [16]
Для совместного выделения а - и ( 3-пиненов может быть использован одноколонный аппарат. [17]
Для совместного выделения селена и теллура применяют SnCb, соли гидразина или же раствор SCb и соли гидразина. [18]
Перенапряжение совместного выделения хлора и кислорода на двуокиси марганца подчиняется законам электрохимической кинетики, а коэффициенты а и Ъ уравнения Тафеля не выходят за пределы величин для электрохимических реакций. [19]
При совместном выделении натрия и алюминия, происходящем при катодном процессе, натрий диффундирует через расплав алюминия и поглощается угольными блоками. При этом происходит разбухание блоков, поскольку атомы натрия проникают в пространство между гексагональными решетками атомов углерода и раздвигают их. При этом важное значение имеет концентрация фторида натрия в электролите. С возрастанием концентрации NaF ( ростом криолитового отношения) заметно повышается содержание натрия, растворенного в алюминии и поглощенного угольной футеровкой. [20]
При совместном выделении тепла и влаги параметры приточного и уходящего воздуха связаны между собой влажностно-тепловым балансом. При высоких значениях углового коэффициента г) влажность удаляемого воздуха бывает сплошь и рядом значительно ниже допустимой по санитарным нормам. Другими словами, основным критерием, определяющим параметры уходящего воздуха, является не влажность, а температура. [21]
При совместном выделении газа с водой или нефтью дебит последних также нужно определять. [22]
При совместном выделении смолы и подсмольной воды при процессе полукоксования получают подсмольную воду, имеющую концентрацию отравляющих веществ ( плотного остатка) в 5 - 10 раз ббльшую, чем воды коксохимического завода. [23]
При совместном выделении металлов и водорода соотношение их количеств зависит от концентраций их ионов. Если по условиям опыта по мере осаждения металла концентрация его ионов в растворе уменьшается, а кислотность не падает, то осаждение металла затрудняется, и создаются условия для преимущественного выделения водорода. При очень малых концентрациях такие металлы часто совсем не выделяются из кислых растворов. [24]
Помимо реакций совместного выделения СаС03 и Mg ( OH) 2, происходит взаимодействие их с примесями, обусловливающими мутность и цветность воды. Вследствие малых количеств гидроокись магния не может быть эффективным коагулянтом для этих примесей. Возникает необходимость в добавлении к воде солей алюминия и железа. [25]
Для достижения совместного выделения металлов на катоде могут быть также использованы добавки таких поверхностно-активных веществ, которые вызывают торможение протекания реакции восстановления на катоде более электроположительного компонента. Возникающее при этом повышение перенапряжения разряда ионов этого металла способствует сближению катодных потенциалов выделения обоих металлов. [26]
В случае совместного выделения водорода закономерности распределения тока осложняются вследствие изменения выходов по току металла с плотностью тока, что будет рассмотрено ниже. [27]
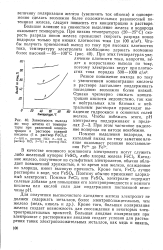 |
Зависимость выхода. [28] |
Большое влияние на совместное выделение железа и водорода оказывает температура. [29]
Недостатком способа является совместное выделение алюминия и A1F3 и трудности выбора стойких материалов для аппаратуры. [30]
Страницы: 1 2 3 4