Аква-комплекс
Cтраница 2
Аквакомплексы образуют только катионы металлов со степенью окисления ( II) и больше, причем способность к образованию аква-комплексов у металлов уменьшается в группах периодической системы сверху вниз. [16]
На этом пути возникают трудности, связанные с низким рН гидратообразования Сг ( ОН) з, инертностью аква-комплексов Cr ( H2O) g, образованием прочных внутриорбитальных комплексов и сложной конструкцией электролизера. [17]
Лигандами могут быть вода, аммиак, амины, галид - и цианид-ионы и др. Медный купорос представляет собой аква-комплекс [ Cu ( H2O) 4 ] S04 - H20, в котором вокруг иона меди координируется четыре молекулы воды, а пятая связана с сульфат-ионом. [18]
При растворении в воде соли типа А1С13 или CuSO4 происходит гидролиз по катиону, ведущий к образованию гидроксо - и аква-комплексов катиона или его основания и к накоплению в растворе ионов гидроксония. [19]
Важнейшими комплексными соединениями с нейтральными лигандами являются аммиакаты ( например, [ Co ( NH3) e ] Cl3) и аква-комплексы ( например, [ Сг ( Н2О) в ] С13), к которым относятся так называемые кристаллогидраты. [20]
Отсутствие прямой связи между константой равновесия и величиной перенапряжения при восстановлении комплексных ионов металла [37, 38] дает основание предполагать, что и в случае аква-комплекса прочность его также не должна оказывать существенного влияния на протекание электродного процесса. [21]
 |
Сопоставление потенциалов разных электродов в растворах редокс-системы Се4 3. [22] |
В то же время ком-плексообразование с анионами перечисленных кислот для Се3 практически не проявляется, и он присутствует в кислых растворах в основном в виде аква-комплексов. [23]
Спектрофотометрическое определение индивидуальных редкоземельных элементов возможно в растворах, содержащих ( в качестве посторонних ионов) в основном только неорганические анионы, поглощающие лишь в далекой УФ-области спектра, так как молярные коэффициенты погашения аква-комплексов редкоземельных элементов очень незначительны ( табл. 13, 14) и присутствие посторонних компонентов может исказить результаты определения. После выделения суммы редкоземельных элементов в виде окислов их переводят чаще всего в хлориды, так как хлорид-ион поглощает в далекой УФ-области. Избыток соляной кислоты легко удаляется выпариванием раствора, при этом исключается возможность образования комплексов. [24]
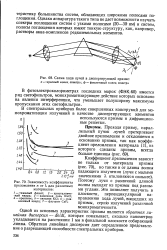 |
Схема хода лучей в диспергирующей призме.| Зависимость коэффициента преломления л от Я для различных. [25] |
Однако аппаратура такого типа не дает возможности изучать спектры поглощения систем с узкими полосами ( 20 - 30 нм) и систем, полосы поглощения которых имеют тонкую структуру, как, например, растворы аква-комплексов редкоземельных элементов. [26]
Снимают спектр поглощения этого раствора по отношению к дистиллированной воде в интервале длин волн от 220 до 1100 нм; первоначально измерения производят через 5 - 10 нм и в области намечающихся максимумов повторяют измерение оптической плотности через 0 5 - 1 нм. Используя спектры поглощения аква-комплексов редкоземельных элементов ( см. рис. 56), устанавливают присутствие отдельных элементов в смеси. [27]
Необходимо также знать, при какой концентрации аква-ион элемента находится в мономерной форме. Сведения о КуСТ аква-комплексов изучаемого иона элемента и их способности к замещению молекул воды на другие лиганды ( их инертности) можно получить, главным образом, из периодической литературы; число таких работ пока не очень велико. [28]
В полученных растворах находятся аква-комплексы, имеющие одинаковую координацию ( окта-эдрическую), но различный цвет. Последнее указывает на разную величину расщепления терма, зависящую от природы центрального атома. В случае Zn ( d10) терм не расщепляется - раствор бесцветный. В случае Mn ( rf5) расщепление тоже мало и раствор имеет очень слабую окраску. [29]
Необходимо также знать, при какой концентрации аква-ион элемента находится в мономерной форме. Сведения о / Суст аква-комплексов изучаемого иона элемента и их способности к замещению молекул воды на другие лиганды ( их инертности) можно получить, главным образом, из периодической литературы; число таких работ пока не очень велико. [30]
Страницы: 1 2 3