Выпадение - гидроксид
Cтраница 1
Выпадение гидроксида железа ( III) окрашивает накипь в желтый цвет. [1]
Выпадение гидроксидов Al ( OH) 3 и Сг ( ОН) 3 объясняется тем, что гидратированные ионы алюминия и хрома, взаимодействуя с водой, ступенчато гидролизуются с образованием малорастворимых гидроксидов. Этому процессу способствует и реакция взаимодействия сульфид-аниона с водой, ведущая к накоплению в растворе свободных гидроксильных ионов. [2]
Выпадение гидроксида железа окрашивает накипь в желтый цвет. [3]
В противном случае могут образовываться алюминаты и выпадения гидроксида алюминия не будет. [4]
Повышение рН раствора до 12 приводит к выпадению гидроксида магния, который может адсорбировать на своей поверхности ионы цинка, что приводит к увеличению погрешности определения. [5]
В этих условиях аммиак образует аммиакат кадмия и выпадение гидроксида кадмия предотвращается. [6]
Аскорбиновая кислота восстанавливает Fe3 до Fe2 и тем самым предотвращает выпадение гидроксида железа. [7]
Установлено, что при обработке смывных вод едким натром ( рН 12) происходит разрушение комплексонатов с выпадением труднорастворимых гидроксидов в осадок. [8]
Зосле нейтрализации в сточных водах содержатся тонкодисперсные нерастворенные загрязнения, которые отстаивают с предварительной коагуляцией при помощи химических реагентов, образующих в воде хлопья. Большое значение при этом имеет рН, при котором обеспечивается полнота гидролиза солей и выпадение гидроксида алюминия. [9]
Полный гидролиз может произойти, если вода для гидратации непрерывно обновляется. При достижении предельной концентрации Са ( ОН) 2 гидратация не прекращается, а происходит выпадение гидроксида кальция из раствора. [10]
Пиридин образует соли с одним эквивалентом кислоты. Он связывает соляную кислоту, образующуюся при гидролизе хлорида железа, сдвигая равновесие этой реакции до выпадения гидроксида железа. [11]
 |
Величины а 4. в растворах с различными рН. [12] |
Определяемый металл часто присутствует в титруемом растворе не только в виде свободного иона Мя или комплекса с ЭДТА MY - 4, но и в виде комплексов с компонентами буферного раствора или гидроксид-ионами. Так, при титровании многовалентных элементов даже в кислой среде могут образовываться гидроксокомплексы. Для предотвращения выпадения гидроксидов металлов к раствору прибавляют вспомогательные комплексообразующие вещества, например аммиак, тартрат, цитрат и другие ионы. Для приготовления буферных смесей используют аммиак, ацетаты и другие соединения, которые также способны образовывать комплексы с ионами металлов. [13]
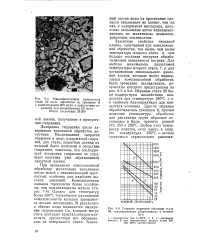 |
Скорость коррозии образцов стали. [14] |
При проведении комплексонной обработки желательно заполнение котла водой с незначительной жесткостью, особенно для наиболее высоких давлений. Однако для температур более 350 С термическое разложение комплексонатов кальция проявляется весьма интенсивно. В результате в объеме воды начинается выпадение гидроксидов Са, которые могут стать центрами кристаллизации магнетита, препятствуя его образованию на поверхности стали. [15]
Страницы: 1 2