Акво-ион
Cтраница 3
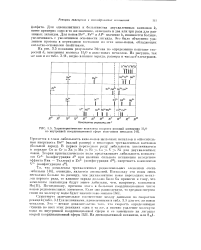 |
Характеристические констант ].. скорости реакций замещения Н20 во внутренней координационной сфере акво-ионов металлов. [31] |
На рис. 3.5 показаны результаты Эйгена по определению констант скоростей kc замещения молекул Ы20 в акво-ионах металлов. Из рисунка, так же как и из табл. 3.11, видно влияние заряда, размера и числа й-электронов. [32]
Ион одновалентного серебра Ag, очевидно, сольватирован в водных растворах, но в твердых солях акво-ион не встречается. [33]
Предложите объяснения для следующих фактов: а) акво-ион никеля ( II) парамагнитен, а акво-ион палладия ( II) диамагнитен. [34]
Таким образом можно вычислить константу устойчивости комплекса триэтилендиаминкобальта ( III), так как окислительно-восстановительный потенциал систем акво-ионов кобальта известен из литературы, а константа устойчивости триэтилендиаминкобальта ( II) - из измерений, приведенных в предыдущей главе. [35]
Таким образом можно вычислить константу устойчивости комплекса триэтилендиаминкобальта ( III), так как окислительно-восстановительный потенциал систем акво-ионов кобальта известен из литературы, а константа устойчивости триэтилендиаминкобальта ( II) - из измерений, приведенных в предыдущей главе. [36]
Особенно это относится к случаю нейтральных или близких к ним сред, где следует ожидать гидролитического отщепления Н от акво-ионов рзэ и их разрядки. [37]
В водном растворе ионы металлов гидратированы большим или меньшим числом молекул воды, но, за некоторым исключением, о составе рассматриваемых акво-ионов ничего определенного неизвестно. Изучением диализа Бринцин-гер [22] пытался провести различие между химически связанной и менее прочно связанной водой в гидратированных ионах металлов. [38]
Во время подготовки этой статьи к печати были получены прямые экспериментальные доказательства того, что обмен в ноне [ РШг4р - идет чероа посредство акво-ионов. [39]
С другой стороны, у металлов первого ряда переходных элементов очень важны состояния окисления II и III, для которых известно большое число комплексов и акво-ионов; в химии тяжелых элементов эти состояния окисления не имеют столь большого значения. [40]
Рассчитанные из констант нестойкости и констант скорости акватации константы скорости обратного вступления ионов хлора в аквокомплексы закономерно возрастают по мере уменьшения отрицательного заряда и повышения положительного заряда акво-иона. Эти реакции описываются уравнением 2-го порядка. [41]
Переходя к соединениям с кислородсодержащими лигандами, надо указать, что C ( IV) и Si ( IV) по причине очень большой силы поля не образуют акво-ионов. Однако кислородные кислоты Н2С03, H2SiO3, H4SiO4 ( как и Н3Р04, H2S04, НСЮ4) вполне закономерно рассматривать как продукты ступенчатой диссоциации соответствующих акво-ионов. [42]
Из данных, приведенных в табл. 27, также можно сделать вывод, что в случае благородногазовых ионов донорно-акцеп-торная связь, невидимому, существенной роли не играет и энергию образования комплексного акво-иона с центральным бла-городногазовым ионом можно рассчитать, пользуясь одними электростатическими представлениями. [43]
Применительно к изучавшимся нами производным четырехвалентной платины внесение поправок на сольватационное равновесие едва ли нужно при высокой прочности этих соединений в смысле констант нестойкости и довольно сильно выраженных кислотных свойствах акво-ионов четырехвалентной платины. Следовательно, чем сильнее поле центрального иона, тем у аммиакатов и аминатов резче должно быть выражено кислотно-основное и слабее - сольватационное равновесие. [44]
Для ускорения каталитической реакции достаточно и того, чтобы образование циклической структуры, показанной в схеме (III.82), вызвало бы ослабление связи О-О более сильное, чем в комплексе HgOa с акво-ионом металла. Тогда взаимодействие такой разрыхленной молекулы HaOg с иодидом ( возможно, в пределах координационной сферы М) будет протекать с большей скоростью, чем в отсутствие активатора. [45]
Страницы: 1 2 3 4