Акво-комплекс
Cтраница 2
Подобно тому как вода может отщепляться от твердых акво-комплексов, так и из амминов металлов иногда можно удалить аммиак и амины. Это общий метод синтеза соединений типа транс - [ PtA2X2 ] - Самым обычным примером является получение транс - [ Р К. [16]
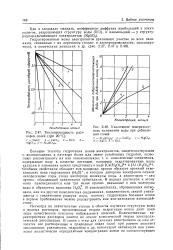 |
Теплопроводность растворов солей ( при 20 С.| Увеличение поверхностного натяжения воды при добавлении солей. [17] |
Особыми свойствами обладает ион водорода: протон образует прочный акво-комплекс иона гидроксония ( Н3О), в котором донорами электронов служат неподеленные пары атома кислорода молекулы воды, а акцептором - сам протон, обладающий вакантными орбиталями. В аквокомплексах, образованных катио-нами, как и в других комплексных соединениях, ковалентность связей уменьшается с увеличением радиуса иона, поэтому гидратацию больших ионов в первом приближении можно рассматривать как ион-дипольное взаимодействие. [18]
Ионы металлов находятся в водных растворах в виде акво-комплексов. Окислительно-восстановительные потенциалы простых ионов по существу неизвестны, и имеющиеся данные относятся к аквокомплексам, в которых лигандом является вода. На величину окислительно-восстановительного потенциала образующего иона большое влияние оказывает химическая природа лигандов. [19]
В табл. 12.7 приведены значения Д для некоторых октаэдри-ческих акво-комплексов первого ряда переходных элементов, а в табл. 12.8 сопоставлены значения А для разных лигандов одного и того же иона металла. [20]
В табл. 12.7 приведены значения А для некоторых октаэдрических акво-комплексов первого ряда переходных элементов, а в табл. 12.8 сопоставлены значения А для разных лигандов одного и того же иона металла. [21]
Соединения, содержащие алшин-комплексы, называются аммиакатами, а содержащие акво-комплексы - гидратами. [22]
Соединения, содержащие аммин-комплексы, называются аммиакатами, а содержащие акво-комплексы - гидратами. [23]
Вода, обладающая высокой активностью при координации и образовании акво-комплексов с ионами переходных металлов, особенно сильно влияет на скорость комплек-сообразования. Это свойство воды отчетливо обнаруживается в реакциях, протекающих в неводной среде. [24]
В кислых водных растворах ионы Be24 находятся в виде прочных акво-комплексов [ Ве ( ОН. [25]
Хорошим примером таких превращений могут служить превращения в ряду акво-комплексов типа цис - и транс - [ Со еп2 АН2О ], легко изомеризующихся и рацемизую-щихся в водном растворе. Если А - Н 2О и NCS, исследование процесса обмена молекулы воды с использованием в качестве метки Н 218О наводит на мысль, что изомеризация действительно является следствием замещения одной молекулы воды другой, приводящего к стереохими-ческому превращению. Эти реакции требуют большего внимания и более тщательного изучения и могут представить значительный интерес. Но в настоящее время мы не располагаем достаточными экспериментальными данными, поэтому дальнейшее обсуждение вести нецелесообразно. [26]
Гидроксокомплексы в водных растворах обычно находятся в равновесии с акво-комплексами. В то время как последние часто склонны к отдаче протонов, в аммиакатах подобный процесс протекает только в редких случаях. [27]
Однако последний пример относится к амминным комплексам, а не к акво-комплексам. [28]
При внешнесферном восстановлении комплекс с гидроксилом, по-видимому, реагирует медленнее, чем соответствующий акво-комплекс ( см. стр. [29]
Реакции типа ( 35) довольно распространены; они были применены для получения акво-комплексов из соответствующих карбонатных комплексов. [30]
Страницы: 1 2 3 4