Выход - алюминий
Cтраница 2
Оптимальными параметрами для обесцвечивания воды с ЦИсх100 град, следует считать: при ДК 0 25ДР - необходимое количество электричества 20 Кл / л, при Дк 0 37 Др - 15 Кл / л и при ДК 0 5ДР - 10 Кл / л; при плотности тока / 10 А / дм2 эффект обесцвечивания снижается. Влияние изменения температуры на обесцвечивание воды и выход алюминия сказывается несущественно. [16]
 |
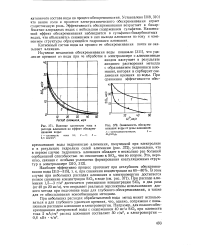
Зависимости выхода алюминия по [ IMAGE ] Влияние плотности тока току Вт от температуры воды при плотно - на скорость растворения алюми-сти тока ния при поляризации. [17] |
Ионный состав воды оказывает сложное влияние на процесс растворения электродов. В присутствии СО3 - - ионов наблюдается торможение анодного процесса, выход алюминия по току не превышает 63 %, SC4 - - ионы замедляют активирующее действие С1 - - ионов, и тем в большей степени, чем больше соотношение между SO. Однако введение даже незначительных количеств С1 - - ионов в воду, содержащую 5О4 - - ионы, активирует процесс растворения алюминия. [18]
Для протекания прямой реакции (2.1) необходимо нейтрализовать образующуюся серную кислоту, что можно осуществить, например, добавлением к раствору оксида и / или гидроксида алюминия. С увеличением молярного отношения A12O3 / SO3 степень гидролиза повышается и выход алюминия в осадок основной соли достигает 100 % при добавлении к раствору сульфата алюминия 62 % А12О3 в виде гидроксида алюминия. [19]
 |
Схема электролизера с засыпными электродами. [20] |
Однако смена полярности тока не всегда эффективна. В период переключения полярности осадки иногда не удаляются и резко падает выход алюминия по току. С увеличением скорости движения воды в межэлектродном пространстве повышается количество растворенного алюминия, уменьшаются поляризация и расход электроэнергии, предотвращается образование оксидной пленки на электродах. Расход электроэнергии понижается при уменьшении расстояния между электродами. Из конструктивных соображений его принимают равным 10 - 16 мм. [21]
Увеличение степени деалюмипирования при обработке Н - морденита растворами HCI после нагревания кристаллов в токе воздуха, насыщенного парами воды, отмеченное в [169], также могло быть связано с переходом части тетраэдрического алюминия каркаса в кати-онное состояние. Авторы считают поэтому, что при термообработке Н - морденита в присутствии пара воды тетра-эдрический каркасный алюминий не переходит в состояние обменного катиона; происходит лишь частичный гидролиз алюминия в тетраэдрах, приводящий к разрыву только одной или двух связей А1 - О - Si, что при последующем действии кислоты облегчает выход алюминия из каркаса. Выход алюминия в раствор NaCl из кристаллов Н - морденита после предварительного нагревания их на воздухе, наблюдавшийся в [158], следует объяснять, по-видимому, переходом каркасного алюминия в состояние обменного гидроксикатиона. [22]
Увеличение степени деалюмипирования при обработке Н - морденита растворами HCI после нагревания кристаллов в токе воздуха, насыщенного парами воды, отмеченное в [169], также могло быть связано с переходом части тетраэдрического алюминия каркаса в кати-онное состояние. Авторы считают поэтому, что при термообработке Н - морденита в присутствии пара воды тетра-эдрический каркасный алюминий не переходит в состояние обменного катиона; происходит лишь частичный гидролиз алюминия в тетраэдрах, приводящий к разрыву только одной или двух связей А1 - О - Si, что при последующем действии кислоты облегчает выход алюминия из каркаса. Выход алюминия в раствор NaCl из кристаллов Н - морденита после предварительного нагревания их на воздухе, наблюдавшийся в [158], следует объяснять, по-видимому, переходом каркасного алюминия в состояние обменного гидроксикатиона. [23]
Строкачу, электрохимическое растворение метал лов состоит из двух основных процессов - анодного и хими ческого растворения в результате взаимодействия с окружаю щей средой. Растворению металла анода способствуют повы шение температуры воды, присутствие в ней ионов-депассива торов, наложение постоянного электрического тока, повышенш скорости движения воды по отношению к поверхности метал ла. Поэтому выход алюминия по току может достигать 120 % i более. В соответствии с теорией электрохимической коррозш при использовании в качестве анода железа или алюминия i природной воде протекают реакции анодного растворения i образования гидроксидов этих металлов. На катоде из желез; или алюминия в природной воде происходят деполяризацю мигрирующими ионами, деполяризация нейтральными молеку лами, восстановление ионов металлов и нерастворимых пле нок, а также органических соединений. Из вышеуказанных катодны: процессов в природной воде главенствующим является водо родная и кислородная деполяризация. [24]
Активность алюминиевого анода также определяется природой и концентрацией присутствующих в воде анионов. Наибольшее влияние на активность алюминиевого анода оказывает хлор-ион. С увеличением температуры воды от 2 до 80 С выход алюминия по току повышается, и особенно резко в интервале 2 - 30 С. При более высоких значениях плотности тока с повышением температуры воды возрастает напряжение на электродах и снижается выход алюминия по току. [25]
Выход металла по току определяется минеральным составом воды. Ионы SC4 - и НСОГ замедляют анодное растворение алюминия. При наличии сульфат-гидрокарбонат - и гидрокар-бонат-сульфат-ионов в растворе наряду со снижением выхода алюминия по току происходит рост напряжения на электродах. Наличие SOii - - ионов в воде вызывает пассивацию алюминиевого анода, что приводит к постепенному снижению силы тока и выхода алюминия. Интенсивное растворение алюминиевого анода протекает при содержании в растворе до 20 % хлоридов от суммы всех анионов. При этом значительно возрастает содержание алюминия в воде за счет активного химического растворения. Повышенное содержание гидроксида алюминия в воде обеспечивает эффективную очистку воды от загрязнений. [26]
 |
Влияние плотности тока и расхода алюминия на эффект обескремнивания воды.| Зависимость обескремнивания воды от дозы алюминия. [27] |
Установлено [309, 310] что анион соли в процессе электрохимического обескремнивания играет существенную роль. Эффективность обескремнивания возрастает в бикар-бонатно-хлоридных водах с небольшим содержанием сульфатов. Наименьший эффект обескремнивания наблюдается в сульфатно-бикарбонатных водах, что объясняется снижением в них выхода алюминия по току и изменением структуры образующейся гидроокиси алюминия. [28]
Превращение алюминия в катион связано с процессом, известным под названием стабилизация цеолитов. Ультрастабильная форма цеолита Y, полученная термическим разложением аммонийной формы в парах воды, обнаруживает повышенную термическую стабильность. Вполне вероятно, что обычный процесс дегидроксилирования, описанный в этой главе, может сопровождаться выходом алюминия из каркаса и образованием дефектов, обусловливающих возникновение нестабильной структуры ( см. разд. [29]
В таких электролитах анодный процесс сложный. Наряду с растворением алюминия происходит газовыделение на аноде, способствующее его пассивации. В эфирно-гидридных электролитах выделяется водород, причем его выделение наблюдается даже при 100 % - ном выходе алюминия. Высказано мнение, что газовыделение на аноде можно объяснить самопроизвольным разложением гидридного аниона под воздействием свежеобразующейся поверхности алюминия [298], Еще более обильное газовыделение наблюдается на инертных анодах, например платине, где разряд гидридного водорода является основным процессом. [30]
Страницы: 1 2 3