Выход - антибиотик
Cтраница 1
Выход антибиотика резко повышается. [1]
В прошлом для увеличения продуктивности штаммов обычно использовали мутагенез и отбор: именно таким путем удалось повысить выход антибиотиков, синтезируемых гриба ми и акти-номицетами. Было последовательно отобрано свыше двадцати штаммов, продуцирующих все больше пенициллина, и в конечном счете продуктивность увеличилась в 55 раз. [2]
Исходя из факта, что грамицидин является основанием, мы применили новый метод выделения его из исходной сухой плесени; при этом оказалось, что выход антибиотика удалось поднять до 54 % к весу сухих бактериальных тел. Этот метод далеко превзошел ранее разработанный метод экстракции подкисленным этиловым спиртом с последующим использованием 4 % - ного раствора для клинических целей. [3]
Многое вещества ( масла, жиры, спирты и др.) - пеногасители, потребляются продуцентами антибиотиков как дополнительные источники углеродного питания. При этом часто наблюдается повышение выхода антибиотика. Однако внесение пеногасителя снижает скорость потребления кислорода, что в свою очередь может отрицательно сказаться на развитии микроорганизма и его биосинтетической активности. [4]
Биосинтез тетраена антимикоина стимулируется ионами кальция и магния, амфотерицина В - ионами марганца, никеля, цинка, кобальта. При изучении стимулирующего влияния железа, цинка и магния на биосинтез кандицидина максимальный эффект на комплексной среде наблюдается, когда концентрация добавок составляет 5ХЮ - 4 - Ю-3 М, причем увеличение выхода антибиотика сопровождается уменьшением накопления биомассы. Выявлено различие концентраций, оптимальных для роста продуцентов и для биосинтеза антибиотиков. [5]
Обработка гетерофлокулянтами культуральных жидкостей феноксиметилпенициллина и неомицина в концентрациях ОД и 0 05 % соответственно в 1 5 раза увеличивает скорость их фильтрования и в 2 - 2 5 раза снижает пигментацию нативныхрастворов. ФАВ-16 снижает количество применяемого дезэмульгатора в 3 раза и уменьшает потребность в активном угле. Обработка гетерофлокулянтами культуральной жидкости неомицина на 10 - 12 % увеличивает выход антибиотиков в сравнении с контролем и позволяет исключить из технологической цепочки коагулянты СаС12 и тринатрийфосфат. [6]
Однако в технике и в быту образование пены очень часто вызывает немало осложнений и забот. Она нарушает работу котлов высокого давления и магистральных трубопроводов для жидкостей, снижает эффективность работы сахарных и бумажно-целлюлозных заводов. Пена портит кинопленку и ухудшает качество окраски тканей, выводит из строя автоматику и снижает выход антибиотиков на заводах медпрепаратов. Один пузырек газа в аппарате искусственного кровообращения может стать причиной смерти больного на операционном столе. [7]
Вследствие плохой растворимости кислорода в воде и высокой плотности культуры Streptomyces его часто оказывается недостаточно, рост клеток замедляется и выход антибиотика снижается. Чтобы решить эту проблему, можно, во-первых, изменить конструкцию биореакторов, в которых выращивается культура Streptomyces, а во-вторых, используя методы генной инженерии, создать штаммы Streptomyces, более эффективно использующие имеющийся кислород. Эти два подхода не исключают друг друга. [9]
 |
Влияние дополнительных копий rpoD - гена Pseudomonas fluorescens CHAD на способность этой бактерии защищать корни растений огурца от повреждений, вызываемых патогенным грибом Pythium ulti. [10] |
Способность бактерий, стимулирующих рост растений, подавлять пролиферацию фитопатогенов можно повысить, если ввести в эти бактерии гены, кодирующие биосинтез антибиотиков, которые обычно синтезируются другими бактериями. Это позволит расширить спектр фитопатогенов, рост которых способна подавлять одна бактерия. Более того, ограничивая размножение других почвенных микроорганизмов, секретирующие антибиотик бактерии, стимулирующие рост растений, облегчают свою собственную пролиферацию, поскольку уменьшается число конкурентов за ограниченные пищевые ресурсы, а с помощью методов генной инженерии со временем удастся увеличить выход бактериальных антибиотиков. [11]
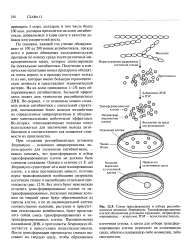 |
Схема трансформации и отбора рекомбинантных штаммов Streptomyces. Трансформированные клетки обозначены розовыми кружками, нетрансформированные - зелеными. ПЭГ - полиэтиленгликоль. [12] |
По оценкам, каждый год ученые обнаруживают от 100 до 200 новых антибиотиков, прежде всего в рамках обширных исследовательских программ по поиску среди тысяч различных микроорганизмов таких, которые синтезировали бы уникальные антибиотики. Получение и клинические испытания новых препаратов обходятся очень дорого, и в продажу поступают только те из них, которые имеют большую терапевтическую ценность и представляют экономический интерес. На их долю приходится 1 - 2 % всех обнаруживаемых антибиотиков. Большой эффект здесь может дать технология рекомбинантных ДНК. Во-вторых, генноинженерные подходы могут использоваться для увеличения выхода антибиотиков и соответственно для снижения стоимости их производства. [13]
Оказалось, что активность ферментов ГМФ-пути ( глюкозо-6 - фосфатдегидрогеназы, фосфоглюконат-дегидрогеназы и транскетолазы) у продуцента нистатина в 2 - 4 раза выше, чем у неактивного мутанта. Особенно эта разница велика во вторую фазу роста культур, когда начинается образование и накопление нистатина в мицелии. Автор считает, что высокая активность ферментов ГМФ-пути расщепления Сахаров является одним из необходимых условий для биосинтеза нистатина. Предполагается, что связующим звеном между механизмами диссимиляции Сахаров и образованием антибиотика может быть восстановленный НАДФ. Управление биосинтезом нистатина, по мнению автора, может осуществляться изменением соотношения активности ферментов, принимающих участие в расщеплении углеводов, что позволй ет в 1 5 - 2 раза увеличить выход антибиотика. [14]
Страницы: 1
